![]()
ЁОБОНВНЬг§аХЯЂЁП
вЛ. НЬбЇФкШнЃК
СђЕФЛЏКЯЮя
Жў. НЬбЇФПБъ
1. жЊЪЖгыММФмФПБъ
ЃЈ1ЃЉеЦЮеСђЕФбѕЛЏЮяSO2ЕФаджЪЃЌгУЭОКЭЮЃКІЃЛ
ЃЈ2ЃЉдкЯЁСђЫсЕФЛљДЁЩЯЃЌеЦЮеХЈСђЫсЕФЕФЬиад.
2. Й§ГЬгыЗНЗЈФПБъ
ХрбјбЇЩњЕФЙлВьФмСІКЭЫМЮЌФмСІЃЌЭЦРэЬНОПФмСІЁЃ
3. ЧщИаЬЌЖШгыМлжЕЙлФПБъ
ЖдбЇЩњНјааБчжЄЮЈЮяжївхЙлЕуЕФНЬг§ЃЌМЄЗЂбЇЯАаЫШЄЃЌХрбјбЇЩњбЯНїЧѓЪЕЕФПЦбЇзїЗчЁЃ
Ш§. НЬбЇжиЕуЁЂФбЕу
1. SO2ЕФЛЏбЇаджЪЃЛ
2. ХЈСђЫсЕФЬиадЁЃ
ЫФ. НЬбЇЗНЗЈ
ЁЁЁЁЬжТлЃЋЬНОПЃЋЪЕбщ
ЃлНЬбЇЙ§ГЬЃн
ПеЦјжЪСПШеБЈ
|
ГЧЪаУћГЦ |
ЮлШОжИЪ§ |
ЪзвЊЮлШОЮя |
ПеЦјжЪСПМЖБ№ |
ПеЦјжЪСПзДПі |
|
ББОЉ |
60 |
ПЩЮќШыПХСЃЮя |
Ђђ |
СМ |
|
ЬьНђ |
68 |
ЖўбѕЛЏСђ |
Ђђ |
СМ |
|
ЩЯКЃ |
69 |
ПЩЮќШыПХСЃЮя |
Ђђ |
СМ |
|
ФЯОЉ |
77 |
ПЩЮќШыПХСЃЮя |
Ђђ |
СМ |
|
ГЄЩГ |
78 |
ЖўбѕЛЏСђ |
Ђђ |
СМ |
|
жщКЃ |
46 |
ЁЁ |
Ђё |
гХ |
|
ЩЧЭЗ |
37 |
ЁЁ |
Ђё |
гХ |
|
РМжн |
175 |
ПЩЮќШыПХСЃЮя |
Ђѓ2 |
ЧсЖШЮлШО |
ЯыЯыЃКФуСЫНтЖўбѕЛЏСђгаЖрЩйЃП
вЛЁЂЖў бѕ ЛЏ Сђ
1ЁЂЮяРэаджЪЃЛЮоЩЋДЬМЄадЦјЮЖЕФгаЖОЦјЬхЃЌвзШмгкЫЎ
SO2ФмЗёШмгкЫЎ?
ЬНОПЪЕбщ1ЃК
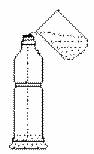
ЯђвЛИіЪеМЏТњЖўбѕЛЏСђЦјЬхЕФЫмСЯЦПжаМгШывЛЖЈЬхЛ§ЕФЫЎЃЌСЂМДИЧЩЯЦПИЧЁЃ
|
ЪдбщЯжЯѓ |
ЫмСЯЦПБЛБфБёСЫ |
|
ЗжЮі |
ЦПРябЙЧПМѕаЁЃЌжЄУїЖўбѕЛЏСђШмгкЫЎ |
2. ЛЏбЇаджЪ
ЃЈ1ЃЉдйЯыЯы
ИљОнЖўбѕЛЏСђЕФдЊЫизщГЩКЭдЊЫиЕФЛЏКЯМлЃЌФуФмдЄВтЫќгаФФаЉаджЪТ№ЃП
ЃЈ2ЃЉЬжТл
ЩшМЦЪЕбщЬНОПЖўбѕЛЏСђЕФЛЏбЇаджЪ
SO2гыЫЎгаУЛгаЗЂЩњЛЏбЇЗДгІ?
ЬНОПЪЕбщ2ЃК
ЯђЭЈШыСЫSO2ЕФЫЎжаМгШызЯЩЋЪЏШяЪдвК
|
ЪдбщЯжЯѓ |
зЯЩЋЪЏШяЪдвКБфКь |
|
ЗжЮі |
ШмвКжагаHЃЋЃЌгааТЮяжЪЩњГЩ. |
SO2ЃЋH2OЃНH2SO3
![]()
H2SO3ЪЧЗёЮШЖЈ?
ЬНОПЪЕбщ3ЃК
дкH2SO3ЩЯЗНЗХвЛеХPHЪджНЃЌ
|
ЪдбщЯжЯѓ |
PHЪджНБфКь |
|
ЗжЮі |
гаSO2ЩњГЩ |
H2SO3 ЃН SO2ЁќЃЋH2O

аЁНсЃКSO2ЃЋH2O![]() H2SO3
H2SO3
ЫМПМЃК ФмЗёгУЫЎРДЮќЪеSO2
вђЮЊSO2ЮЊПЩФцЃЌЫљвдгУЫЎРДЮќЪеВЛГЙЕз.
ПЩвдгУЪВУДРДЮќЪеSO2?
SO2ЃЋ2NaOHЃНNa2SO3ЃЋH2O
ЬНОПЪЕбщ4ЃК
|
ЪЕбщВНжш |
ЯжЯѓ |
НсТл |
|
ЭљзАгаSO2ЕФеыЭВФкГщШЁ0.5mLЦЗКьШмвКЃЌгУЯ№НКШћЗтКУКѓЩЯЯТвЁдШ |
ЦЗКьШмвКЭЪЩЋ |
SO2гаЦЏАззїгУ |
|
АбеыЭВФквКЬхзЊвЦЕНаЁЩеБФкМгШШ |
ШмвКБфЛиКьЩЋ |
БЛSO2ЦЏАзВЛЮШЖЈЃЌШнвзБфЛидРДЕФбеЩЋ |
|
дкЩеБПкЗХвЛПщЛЈАъ |
ЛЈАъЭЪЩЋ |
ШмвКжиаТЗжНтГіSO2 |
аЁНсЃК
1ЁЂгыЫЎЗДгІ SO2ЃЋH2O ![]() H2SO3
H2SO3
2ЁЂгыМюадбѕЛЏЮяКЭМюЗДгІ SO2ЃЋNa2OЃНNa2SO3
SO2ЃЋ2NaOHЃНNa2SO3ЃЋH2O
3ЁЂбѕЛЏад 2H2S ЃЋ SO2 ЃН 3SЁ§ ЃЋ 2H2O
4ЁЂНЯЧПЕФЛЙдадЃЈгыCl2ЁЂO2ЁЂFe3ЃЋЕШЃЉ
2SO2 ЃЋ Cl2 ЃЋ H2O ЃН H2SO4 ЃЋ 2HCl
5ЁЂЦЏАзад
ЖСвЛЖС
АзФОЖњгжНавјЖњЃЌЪєецОњРрЪГЦЗЃЌОпгаЩњНђЁЂжЙПШЁЂНЕЛ№ЕШЙІаЇЁЃЕЋвЛаЉВЛЗЈЩњВњепЃЌЮЊСЫЕУЕНИќАзЕФвјЖњЃЌдкДѓХяФкЗХжУСЫСђЛЧЃЌВЩгУетжжДЋЭГЕФЁАСђЛЧбЌеєЁБЙЄвеЩњВњГіРДЕФвјЖњЭљЭљЛсВаСєвЛЖЈСПЕФЖўбѕЛЏСђЁЃФПЧАЃЌЩЯКЃжЪМрВПУХЖдвјЖњВњЦЗНјааСЫвЛДЮзЈЯюГщВщЃЌНсЙћЗЂЯжБЛГщМьЕФ21жжвјЖњВњЦЗОгШЛШЋВПДцдкЖўбѕЛЏСђВаСєСПГЌБъЕФЯжЯѓЁЃВПЗжвјЖњВњЦЗЕФЖўбѕЛЏСђВаСєСПОгШЛИпДя2.83g/kgЃЌзюЕЭЕФЖўбѕЛЏСђВаСєСПвВга0.125g/kgЁЃЮвЙњЁЖЪГЦЗЬэМгМСЪЙгУЮРЩњБъзМЁЗЖдЪГЦЗжаЖўбѕЛЏСђЕФдЪаэВаСєСПзіСЫЧПжЦадЕФЙцЖЈЃЌИљОнетвЛБъзМЃЌвјЖњВњЦЗжаВЛЕУКЌгаЖўбѕЛЏСђВаСєЁЃвђДЫвјЖњВЂЗЧдНАздНКУЁЃ
Ьж Тл
ЖўбѕЛЏСђЕФаджЪОіЖЈСЫЫќгаФФаЉгУЭОКЭЮЃКІФиЃП
ЃЈ1ЃЉЖўбѕЛЏСђЕФгУЭО
AЁЂжЦСђЫс
BЁЂЦЏАзжННЌЁЂУЋЁЂЫПЁЂВнУБ
CЁЂЩБОњЯћЖО
ЃЈ2ЃЉЖўбѕЛЏСђЕФЮЃКІ
AЁЂЖдШЫЬхНЁПЕдьГЩжБНгЮЃКІ
BЁЂаЮГЩЫсгъЁЊЁЊЁАПежаЫРЩёЁБ
аЮГЩЫсгъЕФЭООЖЃК
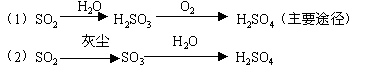
2SO2 ЃЋ O2 ![]() 2SO3
2SO3
SO3 ЃЋ H2O ЃН H2SO4

ЖрХЕРЪТМўЃК
ЖрХЕРЪЧУРЙњБіЯІЗЈФсбЧжнЕФвЛИіГЧеђЁЃ1948Фъ10дТ26жС31ШеЃЌКгЙШЕиДјГжајДѓЮэЬьЦјЃЌЪЙДѓЦјжаЖўбѕЛЏСђХЈЖШДя0.5 ~ 2.0ppmЃЌВЂДцдкУїЯдГОСЃЁЃШЋеђга5911ШЫгаблЁЂБЧЁЂКэДЬМЄжЂзДЃЌВЂАщгааиЭДЁЂКєЮќРЇФбЁЂОчСвЭЗЭДКЭЖёаФЁЂХЛЭТЕШжЂзДЃЌЫРЭі17ШЫЁЃетЪЧУРЙњзюДѓвЛДЮДѓЦјЮлШОЪТМўЁЃЪЧЪРНчАЫДѓЙЋКІжЎвЛЁЃ
ТзЖибЬЮэЪТМўЃК
1952Фъ12дТ5ШежС8ШеЃЌгЂЙњТзЖиЩЯПеСЌајбЬЮэУжТўЃЌбЬГОООУВЛЩЂЃЌДѓЦјжабЬГОХЈЖШИпДя4.46mgЃЏm3ЃЌЖўбѕЛЏСђДя3.8mgЃЏm3ЁЃЮТЖШФцдіЃЌФцЮТВудк40Ѓ15mЕЭПеЁЃдьГЩ4ЬьжаЫРЭіШЫЪ§НЯГЃФъЭЌЦкЖрЫР4000ШЫЃЌетвВЪЧе№ОЊвЛЪБЃЌЮХУћЪРНчЕФАЫДѓЙЋКІжЎвЛЁЃ

ФужЊЕРТ№ЃП
6дТ5ШеЕФЪРНчЛЗОГШеЁЊЁЊ1983ФъжїЬтЃК
ЙмРэКЭДІжУгаКІЗЯЦњЮяЃЌЗРжЮЫсгъ ЦЦЛЕКЭЬсИпФмдДРћгУТЪ
ПЮКѓзївЕЃК
ЕуЛї www.kepu.com.cn ВщдФзЪСЯВЂЛиД№
ЃЈ1ЃЉПеЦјжаSO2ЕФжївЊРДдД?
ЃЈ2ЃЉШчКЮЗРжЙSO2ЮлШОЛЗОГ?
ЬжТл
1ЁЂSO2ФмЪЙТШЫЎЁЂKMnO4ШмвКЭЪЩЋгыSO2ЪЙЦЗКьЭЪЩЋЃЌЪЕжЪЯрЭЌТ№?
2ЁЂдкГБЪЊЬѕМўЯТЃЌШєНЋЕШЮяжЪЕФСПЕФSO2ЦјЬхКЭCl2ЭЌЪБзїгУгкгаЩЋЮяжЪЃЌЦЏАзаЇЙћЛсИќКУТ№?ЮЊЪВУД?
3ЁЂCO2КЭSO2дкЛЏбЇаджЪЩЯМШгаЯрЫЦадгжгаВювьадЃЌШчКЮгУЛЏбЇЗНЗЈМјБ№етСНжжЦјЬхФиЃП
ЖўЁЂСђ Ыс
ИДЯАЃКЯЁСђЫсОпгаФФаЉЫсЕФЭЈадЃП
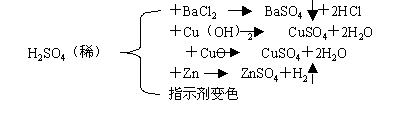
ХЈСђЫс
ЃЈвЛЃЉЮяРэаджЪ
СђЫсЪЧвЛжжЩЋзДЬхЁЃГЃгУЕФХЈСђЫсжаH2SO4ЕФжЪСПЗжЪ§ЮЊ______ЃЌШєЦфУмЖШЮЊ1.84g/cm3ЃЌдђЦфЮяжЪЕФСПХЈЖШЮЊ_____mol/LЁЃСђЫсЪЧвЛжжИпЗаЕу______ЛгЗЂЕФЫсЃЌ___ШмгкЫЎЃЌФмвд_____БШгыЫЎЛьШмЁЃХЈСђЫсШмНтЪБЪЭЗХДѓСПЕФШШЃЌвђДЫЯЁЪЭХЈСђЫсЕФЪБКђвЛЖЈвЊНЋХЈСђЫсТ§Т§зЂШыЫЎжаВЂВЛЖЯНСАш ЃЈЮЊЪВУДЃПЃЉЁЃ
ЃЈЖўЃЉХЈСђЫсЕФЬиадЃК
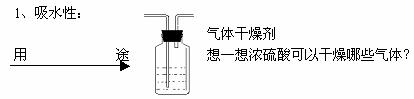
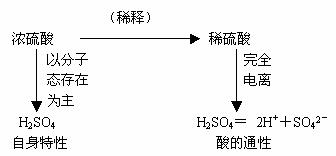
2ЁЂЭбЫЎадЃК
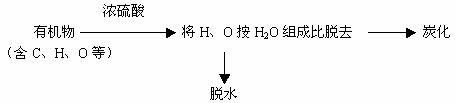
C12H22O11ЃЈесЬЧЃЉ![]() 12C ЃЋ 11H2O
12C ЃЋ 11H2O
ЯывЛЯыЃП
есЬЧЭбЫЎКѓЮЊКЮБфЕУЪшЫЩЖрПзЃП
3ЁЂЧПбѕЛЏад
ЃЈ1ЃЉгыФГаЉЙЬЬЌЗЧН№ЪєЕЅжЪЕФЗДгІЃК
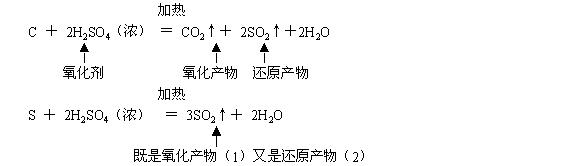 ЃЈ2ЃЉгыН№ЪєЗДгІ
ЃЈ2ЃЉгыН№ЪєЗДгІ
гыЭЗДгІЃЈбнЪОЪЕбщЃЉ
Cu ЃЋ 2H2SO4ЃЈХЈЃЉ![]() CuSO4ЃЋ SO2 ЃЋ2H2O
CuSO4ЃЋ SO2 ЃЋ2H2O
Ђй 1molCu КЭ2molH2SO4ЃЈХЈЃЉЙВШШФмЗёЕУЕН1molSO2?
ЂкХЈСђЫсЕФзїгУЃП
ЯывЛЯыЃП
ЙЄвЕЩЯЮЊКЮФмгУТСВлГЕЪЂЗХЁЂдЫЪфХЈСђЫсЃП
аЁНсЃКСђЫсЕФаджЪ
1ЁЂЯЁСђЫсКЭН№ЪєЗДгІ
2ЁЂХЈСђЫсКЭН№ЪєЗДгІ
3ЁЂХЈСђЫсЕФЬиад
Ш§ЁЂСђЫсЕФгУЭОЃК
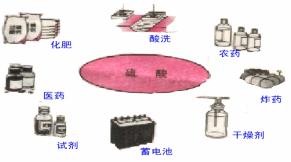
ЫМПМЬтЃК
ЯТСаЯжЯѓЬхЯжСЫСђЫсЕФФФаЉаджЪЃП
ЃЈ1ЃЉАбХЈСђЫсЕЮШыЗХдкеєЗЂУѓРяЕФесЬЧЩЯЃЌесЬЧОЭЛсЬПЛЏБфКк
ЃЈ2ЃЉАбХЈСђЫсТЖжУдкПеЦјРяЃЌжЪСПЛсдіМг
ЃЈ3ЃЉАбаПСЃЗХШыЯЁСђЫсРяЃЌЛсВњЩњЧтЦјЁЃ
ЃЈ4ЃЉАбЭЦЌЗХШыХЈСђЫсРяВЂМгШШЃЌЛсВњЩњSO2ЁЃ
ЃЈ5ЃЉРћгУХЈСђЫсКЭЪГбЮЙЬЬхЗДгІЃЌжЦHClЦјЬхЁЃ
ЁОФЃФтЪдЬтЁП
вЛЁЂВЛЖЈЯюбЁдёЬт
1. НЋSO2ЦјЬхЭЈШыЯТСазуСПШмвКжаЃЌгааТЦјЬхЗДгІЗХГіЕФЪЧЃЈ ЃЉ
A. фхЫЎ B. ЫсадKMnO4 C. ХЈHNO3 D. CuSO4ШмвК
2. ЯТСаЖдSO2КЭSO3ЕФа№Ъіе§ШЗЕФЪЧЃЈ ЃЉ
A. ЭЈГЃЬѕМўЯТЖМЪЧЮоЩЋЦјЬхЃЌЖМвзШмгкЫЎ
B. ЖМЪЧЫсадбѕЛЏЮяЃЌЦфЫЎШмвКЖМЪЧЧПЫс
C. ЖМПЩЪЙЦЗКьШмвКЭЪЩЋ
D. ЖМФмгыМюШмвКЗДгІ
3. ЯТСаЗДгІВЛЪєгкПЩФцЗДгІЕФЪЧЃЈ ЃЉ
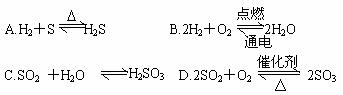
4. ЯТСаЗДгІВњЩњЕФЦјЬхЭЈШыNa2SO3ШмвКЃЌВЛФмЗДгІЕФЪЧЃЈ ЃЉ
A. COЭЈЙ§МгШШЕФCuO B. гЉЪЏгыХЈH2SO4ЙВШШ
C. ХЈH2SO4КЭMgCl2ЙЬЬх D. FeSКЭЯЁH2SO4
5. дкПеЦјжаВЛвзБфжЪЕФЪЧЃЈ ЃЉ
A. Na2SO3 B.
NaHSO4 C.
бЧСђЫс D.
ЧтСђЫс
6. вдЯТЦјЬхФмгУNaOHЙЬЬхИЩдяЕФЪЧЃЈ ЃЉ
A. NH3 B.
SO2 C.
CO2 D.
HClЊЅ
7. ЯТСаЙигкХЈH2SO4ЕФа№ЪіжаЃЌДэЮѓЕФЪЧЃЈ ЃЉ
A. ГЃЮТЯТПЩЪЙФГаЉН№ЪєЖлЛЏ
B. ОпгаЭбЫЎадЃЌЙЪФмзїИЩдяМС
C. МгШШЬѕМўЯТПЩгыФОЬПЗДгІЃЌЦфЛЙдВњЮяЮЊCO2ЁЂSO2
D. ШмгкЫЎЗХГіДѓСПЕФШШ
8. дкЯТЪіЗДгІжаЃЌХЈH2SO4МШБэЯжГібѕЛЏадЃЌгжБэЯжГіЫсадЕФЪЧЃЈ ЃЉ
A. CЃЋH2SO4 B. H2SЃЋH2SO4 C. NaClЃЋH2SO4 D. CuЃЋH2SO4
9. зуСПЕФаПКЭЯТСаЫсЗДгІЃЌВњЩњH2ЕФЮяжЪЕФСПзюЖрЕФЪЧЃЈ ЃЉ
A. 10mL 18.4mol/L H2SO4 B. 30mL 3mol/LбЮЫс
C. 30mL 2mol/L H2SO4 D. 30mL 5mol/L HNO3
10. ЯТСаИїзщЦјЬхЃЌЪЕбщЪвПЩгУСђЫсжЦШЁЃЌгжФмгУХЈH2SO4ИЩдяЕФЪЧЃЈ ЃЉ
A. HClЁЂHBrЁЂHI B.
H2SЁЂCO2ЁЂH2
C. H2ЁЂSO2ЁЂHCl D. NH3ЁЂHFЁЂH2
11. зуСПЕФХЈH2SO4КЭmgЭЭъШЋЗДгІЃЌЕУЕНБъзМзДПіЯТЕФn LSO2ЃЌдђБЛЛЙдЕФСђЫсЪЧЃЈ ЃЉ
A. ![]() B.
B.
![]() C.
C.
![]() D.
D.
![]()
12. жЛгУвЛжжЪдМСОЭФмМјБ№Na2SЁЂNa2SO3ЁЂNa2CO3ЁЂNa2SO4ЕФЪЧЃЈ ЃЉ
A. BaC2ШмвК B. бЮЫс C. ЦЗКьШмвК D. NH4Cl
13. НЋCuSO4ЁЄ5H2OЗХШыХЈH2SO4жаКѓЃЌбеЩЋБфЮЊЃЈ ЃЉ
A. РЖ B. Кк C. Кь D. АзЊЅ
14. ШєгУХЈH2SO4ЪБВЛЩїеДдкЦЄЗєЩЯЃЌЧхЯДЕФЗНЗЈЪЧЃЈ ЃЉ
A. ЯШгУNaOHжаКЭЃЌдйгУЫЎЯД
B. гУЩДВМВСОЛКѓЭПгЭ
C. гУДѓСПЫЎГхЯД
D. гУВМВСКѓЃЌгУЫЎГхЯДЃЌдйгУNaHCO3ШмвКЃЈ3%Ѓ5%ЃЉГхЯД
ЖўЁЂЬюПеЬтЃК
15. аДГіЗћКЯЯТСаЧщПіЕФЛЏбЇЗНГЬЪНЃК
ЃЈ1ЃЉSO2зїЛЙдМС ЃЛ
ЃЈ2ЃЉSO2зїбѕЛЏМС ЃЛ
ЃЈ3ЃЉSO2МШВЛзїЛЙдМСгжВЛзїбѕЛЏМС ЁЃ
ЃЈ4ЃЉХЈСђЫсМШзїЫсгжзїбѕЛЏМС
16. ФГбЧСђЫсФЦЪдМСвбВПЗжБЛбѕЛЏЃЌЮЊШЗЖЈЫќЕФДПЖШЃЌвЊНјааШчЯТЪЕбщЃКЂйГЦШЁбљЦЗw1g; ЂкНЋбљЦЗШмНтЃЛЂлИјШмвКМгШыЩдЙ§СПЕФбЮЫсЫсЛЏСЫЕФBaCl2ШмвКЃЛЂмЙ§ТЫЁЂЯДЕгЁЂИЩдяГСЕэЃЌГЦЦфжЪСПЮЊw2g.ЪдЛиД№ЃК
ЃЈ1ЃЉBaCl2вЊгУбЮЫсЫсЛЏЕФдвђЪЧ
ЃЈ2ЃЉBaCl2ШмвКвЊЩдЙ§СПЕФдвђЪЧ
ЃЈ3ЃЉХаЖЯВйзїЂлЪЧЗёЭъГЩЕФЗНЗЈЪЧ
ЃЈ4ЃЉХаЖЯГСЕэЪЧЗёЯДОЛЕФЗНЗЈЪЧ
ЃЈ5ЃЉNa2SO3ДПЖШЕФБэЪОЪНЮЊ
Ш§ЁЂМЦЫуЬт
17. 76gСђЫсФЦЁЂбЧСђЫсФЦЁЂбЧСђЫсЧтФЦЕФЛьКЯЮяКЭзуСПЕФСђЫсзїгУвнГіЦјЬх672mLЃЈБъзМзДПіЃЉЃЌЭЌбљжЪСПЕФЛьКЯЮяЧЁКУКЭ24.04mL3.2%ЕФЧтбѕЛЏФЦШмвКЃЈУмЖШЮЊ1.04g/mLЃЉЗДгІЃЌЪдМЦЫу дкЛьКЯЮяжабЧСђЫсФЦЕФжЪСПЗжЪ§.
![]()
ЁОЪдЬтД№АИЁП
вЛЁЂ1.C 2.D
3.B 4.AB 5.B
6.A 7.BC 8.D
9.C 10.C 11.AC 12.B 13.D 14.D
ЖўЁЂ15.ЃЈ1ЃЉSO2ЃЋBr2ЃЋ2H2OЃНH2SO4ЃЋ2HBr
ЃЈ2ЃЉ2H2SЃЋSO2 ЃН3SЁ§ЃЋ2H2O
ЃЈ3ЃЉSO2ЃЋ2NaOH ЃНNa2SO3ЃЋH2O
ЃЈ4ЃЉCu ЃЋ 2H2SO4ЃЈХЈЃЉ![]() CuSO4ЃЋ SO2 ЃЋ2H2O
CuSO4ЃЋ SO2 ЃЋ2H2O
16. ЃЈ1ЃЉЗРжЙBaSO3ЩњГЩЊЄ
ЃЈ2ЃЉЪЙSO42ЃЭъШЋзЊЛЏЮЊBaSO4ЊЄ
ЃЈ3ЃЉШЁЩЯВуЧхвКЩйаэЃЌЕЮМгЯЁH2SO4ЃЌШєгаАзЩЋГСЕэЩњГЩдђВйзїЂлЭъГЩЃЌЗёдђЮДЭъГЩЁЃ
ЃЈ4ЃЉШЁзюКѓМИЕЮЯДвКЃЌЕЮМгAgNO3ЃЌШєЮоГСЕэЃЌвбЯДОЛЃЌЗДжЎЃЌЮДЯДОЛЁЃЊЄ
ЃЈ5ЃЉNa2SO3%ЃНЃлЃЈ233W2Ѓ142W2ЃЉ/233W1ЃнЁС100%ЊЄ
17. 26.5%