4.1��ԭ��ء�
1. ��п��ع㷺�������ֵ��������ĵ�Դ�����ķŵ���̿��Ա�ʾΪ
Ag2O+
Zn+H2O = 2Ag��Zn(OH)2.��طŵ�ʱ������������Ӧ��������
A.
Ag B. Zn C. Ag2O
D. Zn(OH)2
2. ij�����������ᷴӦ�����������ý�����п��ɵ�ԭ����У�пΪ�������ý���
A.�� B.ͭ C.�� D.þ
3. ��������������ǵ�һ�ָ��ܵ���D�D��п���أ���缫��ӦʽΪ��
Zn��2OH����2e������ZnO��H2O��Ag2O��H2O��2e������2Ag��2OH�����ݴ��ж���������
A����������������
B��������������ԭ
C��������������ԭ
D����������������
4. ����ԭ��صķ�Ӧͨ���Ƿ��ȷ�Ӧ���������Ͽ���Ƴ�ԭ��صĻ�ѧ��Ӧ����
A��C(s)+H2O(g)=CO(g)+
H2(g) �� ��H��0
B��Ba(OH)2��8H2O(s)+2NH4Cl(s)=
BaCl2(aq)+ 2NH3��H2O(l)+ 8H2O(l) ��
��H��0
C��CaC2(s)+2H2O(l)��Ca(OH)2(s)+C2H2(g)
�� ��H��0
D��CH4(g)+2O2��CO2(g)+2H2O(l)
�� ��H��0
5. ���й���ԭ��ص�������ȷ����
A��ԭ��ؽ���ѧ��ת��Ϊ����
B��ԭ��ظ��������ķ�Ӧ�ǻ�ԭ��Ӧ
C��ԭ����ڹ���ʱ���������ϲ������Ӳ��������·����
D��ԭ��صĵ缫ֻ�������ֲ�ͬ�Ľ�������
6. ������������������������ߣ��Ͼɵ���ѳ�Ϊһ��ؽ����������⣬�ԷϾɵ�صĴ��� �����˶���Դ�ͻ����Ŀɳ�����չ�����ǶԷϾɵ�صĴ�������ҪĿ����
A. ���յ����ǵĽ�������
B. ���յ���еĶ�������
C. ���յ���е�ʯī�缫
D. ��ֹ����е��ؽ��������ӡ�Ǧ��������ˮԴ����Ⱦ
7. ���й���ԭ��ص������У���������
A��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ��
B���õ������ӵ����ֲ�ͬ����ͬʱ����Һ���У����γ�ԭ���
C����ԭ����У�����������һ���Ǹ���������������Ӧ
D����ԭ����У����������һ����������������ԭ��Ӧ
8. Ϊ��������ɫ���������Ƽ���������2008�걱�����˻������й��Լ�������ȼ�ϵ����������Ϊ���������ܳ��͵������㳵��Ԥ�Ƹó�װ������ɫ�������������ӽ���Ĥȼ�ϵ�أ��乤��ԭ����ͼ��ʾ������������ȷ����
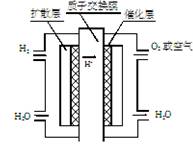
A.ͨ�������ĵ缫����������Ӧ
B.ͨ�������ĵ缫Ϊ����
C.�ܷ�ӦʽΪO2+2H2![]() 2H2O
2H2O
D.�����ĵ缫��ӦʽΪO2+4H+==+4e-2H2O
9.���и�װ���ܹ�����ԭ��ص���
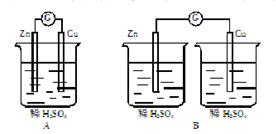
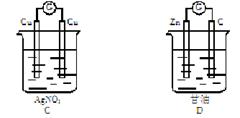
10.ijԭ��ص��ܷ�Ӧ�����ӷ���ʽ�ǣ�Zn+Cu2+==Zn2++Cu���˷�Ӧ��ԭ��ص���ȷ�����
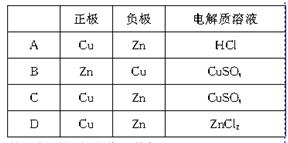
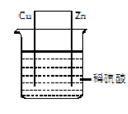
������ͼԭ���װ�õ���������ȷ����
A.ͭ��������ͭƬ�������ݲ��� B.ͭƬ��������
C.������пƬ����������ͭƬ D.��������ͭƬ���汻��ԭ
11. ��п��ع㷺�������ֵ��������ĵ�Դ�����ij��ͷŵ���̿��Ա�ʾΪ��
2Ag+Zn(OH)2![]() Ag2O+Zn+H2O
Ag2O+Zn+H2O
�ڴ˵�طŵ�ʱ�������Ϸ�����Ӧ��������
A.Ag B.Zn(OH)
12. X��Y��Z���ǽ�������X����Z����������Һ�У�X�ı�����Z������X��Y���ԭ���ʱ��YΪ��صĸ�����X��Y��Z���ֽ����Ļ��˳��Ϊ
A.X>Y>Z B.X>Z>Y C.Y>X>Z D.Y>Z>X
13.���������в���ȷ����
A�����ص������Ϸ���������Ӧ�������Ϸ�����ԭ��Ӧ
B��ԭ��ص������Ϸ���������Ӧ�������Ϸ�����ԭ��Ӧ
C�����ʱ����Ƴ�����������Ϸ���������Ӧ
 D����ԭ�������Դ���е��ʱ�����Ӵ�ԭ��ظ��������������
D����ԭ�������Դ���е��ʱ�����Ӵ�ԭ��ظ��������������
14.���и���缫���õ����������ֱ�����Ӧ���ʵ���Һ�У����в������ԭ��ص���
|
|
A |
B |
C |
D |
|
�缫����Һ |
Zn��C���� |
Cu��Ag������ |
Zn��Cu���� |
Mg��Al�������� |
15.���й���ԭ��ص������д������
A.����ԭ��ص������������������ֲ�ͬ�Ľ���
B.ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ��
C.��ԭ����У�����������һ���Ǹ���������������Ӧ
D.ԭ��طŵ�ʱ�������ķ����Ǵ�����������
16.��ͼ��ʾ�����ձ��о�ʢ�к�ˮ���������б���ʴ�ɿ쵽����˳��Ϊ

A.
�ڢ٢ۢ�
B. �ܢۢ٢�
C. �ܢڢ٢�
D. �ۢڢܢ�
17.﮵����һ�������ܵ�أ����������ᡢ�����߶��ܵ����ձ����ӣ�Ŀǰ�����Ƴɹ�����﮵�ء�ij��﮵�ص��ܷ�Ӧʽ��Li��MnO2
�� LiMnO2������˵����ȷ����
A.
Li�Ǹ������缫��ӦΪLi��e-��Li+
B.
Li���������缫��ӦΪLi��e-��Li-
C.
MnO2�Ǹ������缫��ӦΪMnO2��e-��MnO2-
D. ﮵����һ�ֻ����͵��
18.��п�ɵ���ڷŵ�ʱ�ܷ�Ӧ����ʽ���Ա�ʾΪ��
Zn��s����2MnO2��2NH4����Zn2+��Mn2O3��s����2NH3��H2O
�ڴ˵�طŵ�ʱ������̼�����Ϸ�����Ӧ��������
A. Zn B. ̼ C.
MnO2��NH4+ D.
Zn��NH3
19.�ݱ�����п��ؿ���ȡ��Ŀǰ�㷺ʹ�õ�Ǧ���أ���Ϊп�����������û��Ǧ��Ⱦ�����ط�ӦΪ��2Zn��O2��2ZnOԭ��Ϊп�������Һ�Ϳ���������������ȷ����
A.
пΪ�������������븺����Ӧ
B.
������ӦΪZn��2e����Zn2��
C.
��������������Ӧ
D.
���Һ�϶�����ǿ��
 20.�ճ����õĸɵ�صĵ缫�ֱ�Ϊ̼����пƤ���Ժ�״NH4Cl��ZnCl2������ʣ����м���MnO2��������H2��, �缫��Ӧ�ɼ�Ϊ��Zn��2e��==Zn2+��2NH4++2e�� =NH3+H2,�������������ж�����˵����ȷ����
20.�ճ����õĸɵ�صĵ缫�ֱ�Ϊ̼����пƤ���Ժ�״NH4Cl��ZnCl2������ʣ����м���MnO2��������H2��, �缫��Ӧ�ɼ�Ϊ��Zn��2e��==Zn2+��2NH4++2e�� =NH3+H2,�������������ж�����˵����ȷ����
A. �ɵ����пΪ������̼Ϊ����
B. �ɵ�ع���ʱ��������п�������·����̼��
C. �ɵ�س�ʱ����������ʱ����װ��״�����������ʴ�õ���
D. �ɵ�ؿ�ʵ�ֻ�ѧ������ܵ�ת���͵�����ѧ�ܵ�ת��
���������
21. ��װ��ˮ���ձ��У�����(��Ե)����һ����ˮƽ����������������Ӷ��ɵ����ν�����������ƽ��״̬.�����ˮ�м���CuSO4 ��Һ�� (��Һ���ܶȱ仯������)

(1)Ƭ�̺�ɹ۲쵽��������(ָ�����Ľ���Ȧ)
A����Ȧ����Ȧ����ҡ�ڲ���
B������ƽ��״̬����
C����Ȧ������б
D����Ȧ������б
(2)�������������ԭ����__________________________________________________��