![]()
【本讲教育信息】
一、教学内容:
原子结构问题中的重要模型
二、学习目标:
1、知道![]() 粒子散射实验,原子的核式结构模型及玻尔模型的特点。
粒子散射实验,原子的核式结构模型及玻尔模型的特点。
2、理解氢原子的能级结构及特点
3、重点掌握与本部分内容相关的重要的习题类型及相关解法。
三、重难点解析:
(一)原子的核式结构模型:
1. 汤姆生的原子模型
1897年汤姆生用测定粒子荷质比的方法研究阴极射线时发现了电子,电子的发现,对人类认识原子结构有重大的意义,使人们认识到组成物质的微粒――原子也具有复杂结构。由于原子含有带负电的电子,从物质的电中性出发,推想到原子中还有带正电的部分,这就提出了进一步探索原子结构,建立原子模型的问题. 汤姆生的原子模型是在发现电子的基础上建立起来的,汤姆生认为,原子是一个球体,正电荷均匀地分布在球内,电子像枣糕里的枣子一样,镶嵌在原子里面,所以汤姆生的原子模型也叫枣糕式原子结构模型.
注意:汤姆生的原子结构模型虽然能解释一些实验事实,但这一模型很快就被新的实验事实所否定。
2. α粒子散射实验
1909~1911年卢瑟福和他的助手通过做α粒子轰击金箔的实验,获得了重要的发现.
(1)实验装置(如图所示)由放射源、金箔、荧光屏等组成.
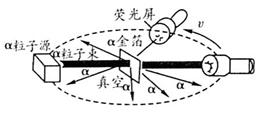
特别提示:①整个实验过程在真空中进行.
②金箔很薄,α粒子(![]() 核)很容易穿过.
核)很容易穿过.
(2)实验现象与结果
绝大多数α粒子穿过金箔后基本上仍沿原来的方向前进,但是有少数α粒子发生了较大角度的偏转。极少数α粒子偏转角超过90°,有的几乎达到180°,沿原路返回,α粒子散射实验令卢瑟福万分惊奇. 若按照汤姆生的原子结构模型去解释:带正电的物质均匀分布,带负电的电子质量比α粒子的质量小得多. α粒子碰到电子就像子弹碰到一粒尘埃一样,其运动方向不会发生什么改变,但实验结果出现了像一枚炮弹碰到一层薄薄的卫生纸被反弹回来这一不可思议的现象. 卢瑟福通过分析,否定了汤姆生的原子结构模型,提出了核式结构模型.
3. 原子的核式结构
卢瑟福依据α粒子散射实验的结果,提出了原子的核式结构:在原子中心有一个很小的核,叫原子核,原子的全部正电荷和几乎全部质量都集中在核里,带负电的电子在核外空间绕核旋转。
问题1、卢瑟福![]() 粒子散射实验现象的理解问题:
粒子散射实验现象的理解问题:
下图为卢瑟福和他的同事们做α粒子散射实验装置的示意图,荧光屏和显微镜一起分别放在图中的A、B、C、D四个位置时,关于观察到的现象,下列说法中正确的是( )
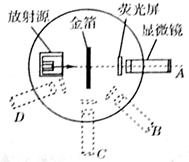
A. 相同时间内放在A位置时,观察到屏上的闪光次数最多
B. 相同时间内放在B位置时,观察到屏上的闪光次数只比放在A位置时稍少些
C. 放在C、D位置时,屏上观察不到闪光
D. 放在D位置时,屏上仍能观察到一些闪光,但次数极少
答案:AD
变式1、
根据α粒子散射实验,卢瑟福提出了原子的核式结构模型。图中虚线表示原子核所形成的电场的等势线,实验表示一个α粒子的运动轨迹,在α粒子从a运动到b、再运动到c的过程中,下列说法中正确的是( )
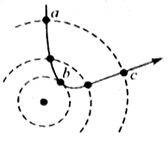
A. 动能先增大,后减小
B. 电势能先减小,后增大
C. 电场力先做负功,后做正功,总功等于零
D. 加速度先变小,后变大
变式2、
1991年卢瑟福依据α粒子散射实验中α粒子发生了____(选填“大”或“小”)角度散射现象,提出了原子的核式结构模型。若用动能为1MeV的α粒子轰击金箔,则其速度约为_____m/s。(质子和中子的质量均为1.67×10-27kg,1MeV=1×106eV)
答案:大,6.9×106
问题2、卢瑟福原子核式结构学说的理解问题
卢瑟福原子核式结构理论的主要内容有( )
A. 原子的中心有个核,叫做原子核
B. 原子的正负电荷都均匀分布在整个原子中
C. 原子的全部正电荷和几乎全部质量都集中在原子核里
D. 带负电的电子在核外绕核旋转
答案:ACD
变式3、
为了探究宇宙起源,“阿尔法磁谱仪”(AMS)将在太空中寻找“反物质”。所谓“反物质”是由“反粒子”构成的。“反粒子”与其对应的正粒子具有相同的质量和相同的电荷量,但电荷的符号相反,则反氢原子是( )
A. 由1个带正电荷的质子和1个带负电荷的电子构成
B. 由1个带负电荷的反质子和1个带正电的正电子构成
C. 由1个带负电的反质子和1个带负电荷的电子构成
D. 由1个不带电的中子和1个带正电荷的正电子构成
答案:B
(二)玻尔的原子模型:
1. 卢瑟福模型与经典电磁理论的矛盾:
注意:①按照经典物理学的观点,带有电荷的电子在轨道上做变速运动,一定会以电磁波的形式向外辐射能量,电子的能量会减小,轨道半径会不断变小,最终落在原子核上,即原子是不稳定的。这与实际情况不符,实际上原子是稳定的。
②按照经典物理学的观点,电子辐射电磁波的频率应等于其振动或圆周运动的频率。由于电子轨道的变化是连续的,辐射电磁波的频率也会连续变化,但实际测定的结果是电磁波的频率不是连续的,同一元素辐射电磁波的频率是分立的某些确定的值。
特别提示:综上所述,微观物体的变化规律不能用从宏观现象中得出的经典理论加以说明,为了解决这一矛盾,丹麦青年物理学家玻尔在前人学说的基础上,把普朗克的量子理论应用于原子系统中,提出了新的原子理论――玻尔的原子理论。
2. 玻尔模型:
(1)量子化模型
玻尔认为,围绕原子核运动的电子轨道半径只能是某些分立的数值,这种现象叫做轨道量子化;不同的轨道对应着不同的状态,在这些状态中,尽管电子在做变速运动,却不辐射能量,因此这些状态是稳定的;原子在不同的状态中具有不同的能量,所以原子的能量也是量子化的。
(2)玻尔理论的两个要点:
①原子只能处于一系列的不连续的能量状态中,在这些状态中原子是稳定的,电子虽然绕核旋转,但并不向外辐射能量,这些状态叫定态。
②原子从一种定态(能量为E1)跃迁到另一种定态(能量为E2)时,它辐射(或吸收)一定频率的光子,光子的能量由这两个定态的能量差决定。即![]()
3. 能级
(1)能级。现代物理学认为,原子的可能状态是不连续的,因此各状态对应的能量也是不连续的。这些能量值叫做能级。
(2)氢原子的能级
对氢原子而言,核外的一个电子绕核运行时,若半径不同,则对应着的原子能量也不同,若使原子电离,原子必须从外界吸收能量,使电子摆脱它与原子核之间的库仑力的束缚,所以原子电离后的能量比原子其他状态的能量都高。我们把原子刚好电离的能量记为0,则其他状态下的能量值就是负的。
原子各级的关系为:
![]()
各状态的标号1、2、3、…叫做量子数,通常用n表示,能量最低的状态叫做基态,其他状态叫做激发态,基态和各激发态的能量分别用E1、E2、E3、…代表。
对于氢原子而言,基态能量:![]()
其他各激发态的能量为:
![]()
(3)能级图
如果用横线表示氢原子的各个能级的能量值,横线间距离表示各能级间的能量值的差,所排列成的阶梯式的图,叫能级图。
氢原子的能级图如图所示,我们应明确:
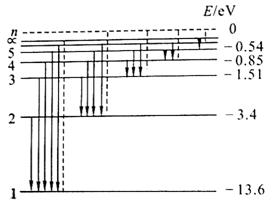
①由能级图可知,由于电子的轨道半径不同,氢原子的能级不连续,这种现象叫能量量子化。②原子的能量包括:原子的原子核与电子所具有的电势能和电子运动的动能。③原子从基态跃迁到激发态时要吸收能量,而从激发态跃迁到基态则以光子的形式向外放出能量,无论是吸收能量还是放出能量,这个能量值不是任意的,而是等于原子发生跃迁时这两个能级间的能级差。即原子吸收光子时是有选择的吸收相应频率的光子。
问题3、原子能级跃迁的计算问题:
已知氢原子基态的电子轨道半径为![]() ,基态的能级值为
,基态的能级值为![]()
(1)求电子在n=2的轨道上运动所形成的等效电流强度;
(2)有一群氢原子处于量子数n=3的激发态,画出一能级图并在图上用箭头表示这些氢原子能发出哪几条光谱线;
(3)计算出这几条谱线中最长的波长。
解析:(1)电子的绕核运转具有周期性,设运转周期为T,由牛顿第二定律和库仑定律可知:![]() 。对轨道上任一处,每一周期通过该处的电量为e,由电流强度的定义式,可求得等效电流强度
。对轨道上任一处,每一周期通过该处的电量为e,由电流强度的定义式,可求得等效电流强度![]() 。联立上述三式可得:
。联立上述三式可得:![]()
(2)由于这群氢原子的自发跃迁辐射,会得到三条谱线,如图所示。
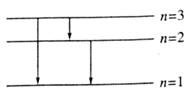
(3)三条光谱线中波长最长的光子能量最小,发生跃迁的两个能级的能量差最小,根据氢原子能级的分布规律可知,氢原子一定是从n=3的能级跃迁到n=2的能级。设波长为λ,由![]()
答案:(1)![]() (2)如上图 (3)
(2)如上图 (3)![]()
变式4、
氢原子的部分能级如图所示。已知可见光的光子能量在1.62eV到3.11eV之间。由此可推知, 氢原子( )
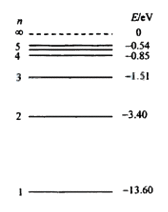
![]()
![]() A. 从高能级向n=1能级跃迁时发出的光的波长比可见光的短
A. 从高能级向n=1能级跃迁时发出的光的波长比可见光的短
![]()
![]() B. 从高能级向n=2能级跃迁时发出的光均为可见光
B. 从高能级向n=2能级跃迁时发出的光均为可见光
![]()
![]() C. 从高能级向n=3能级跃迁时发出的光的频率比可见光的高
C. 从高能级向n=3能级跃迁时发出的光的频率比可见光的高
![]()
![]() D. 从n=3能级向n=2能级跃迁时发出的光为可见光
D. 从n=3能级向n=2能级跃迁时发出的光为可见光
![]() 答案:AD
答案:AD
变式5、
氢原子能级的示意图如图所示,大量氢原子从n=4的能级向n=2的能级跃迁时辐射出可见光a,从n=3的能级向n=2的能级跃迁时辐射出可见光b,则( )
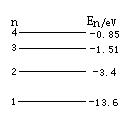
A. 氢原子从高能级向低能级跃迁时可能会辐射出![]() 射线
射线
B. 氢原子从n=4的能级向n=3的能级跃迁时会辐射出紫外线
C. 在水中传播时,a光较b光的速度小
D. 氢原子在n=2的能级时可吸收任意频率的光而发生电离
答案:C
小结:氢原子跃迁、电离的规律以及原子光谱线频率的分析和计算方法。
(1)原子在各能级间跃迁时,所吸收或辐射的光子的能量只能等于两能级间的能级差.
原子电离时所吸收或辐射的光子的能量可以大于或等于某一能级的能量绝对值,即![]() 。
。
说明:![]() 只适用于光子和原子作用而使原子在各定态之间跃迁的情况,对于光子和原子作用而使原子电离,则不受此条件的限制,如:基态氢原子的电离能为13.6eV,只要大于或等于13.6eV的光子都能被基态的氢原子吸收而发生电离,只不过入射光子的能量越大,原子电离后产生的光电子的动能越大.
只适用于光子和原子作用而使原子在各定态之间跃迁的情况,对于光子和原子作用而使原子电离,则不受此条件的限制,如:基态氢原子的电离能为13.6eV,只要大于或等于13.6eV的光子都能被基态的氢原子吸收而发生电离,只不过入射光子的能量越大,原子电离后产生的光电子的动能越大.
(2)入射光子与入射电子的区别与计算:
若是在光子的激发下引起原子的跃迁,则要求光子的能量必须等于原子的某两个能级差;若是在电子的激发下引起原子的跃迁,则要求电子的能量必须大于或等于原子的某两个能级差,要注意两种情况有所不同.
(三)光谱与光谱分析:
1. 发射光谱――物体发光直接产生的光谱。它可分为连续光谱和明线光谱。
①连续光谱――由连续分布的一切波长的光(一切单色光)组成的光谱。炽热的固体、液体和高压气体的发射光谱是连续光谱。如电灯丝发出的光、炽热的钢水发出的光都形成连续光谱。
②明线光谱――只含有一些不连续的亮线的光谱。它是由游离状态的原子发射的,因此也叫原子光谱。稀薄气体或金属的蒸气的发射光谱是明线光谱。实验证明,每种元素的原子都有一定特征的明线光谱。
2. 吸收光谱――高温物体发出的光(其中包含连续分布的一切波长的光)通过物质时,某些波长的光被物质吸收后产生的光谱。如太阳光谱就是太阳内部发出的强光经温度比较低的太阳大气层时产生的吸收光谱。值得注意的是,低温气体原子吸收的光,恰好就是这种原子在高温时发出的光。因此,吸收光谱中的谱线(暗线),也是原子的特征谱线,只是通常在吸收光谱中看到的特征谱线比明线光谱中的少。
3. 光谱分析――由于每种原子都有自己的特征谱线,因此可以根据光谱来鉴别物质和确定它的化学组成,这种说法叫做光谱分析。
做光谱分析时,可以利用发射光谱,也可利用吸收光谱,这种方法的优点是非常灵敏而且迅速。某种元素在物质中的含量达![]() 克,就可以从光谱中发现它的特征谱线将其检查出来。光谱分析在科学技术中有广泛的应用,如检查半导体材料硅或锗的纯度。
克,就可以从光谱中发现它的特征谱线将其检查出来。光谱分析在科学技术中有广泛的应用,如检查半导体材料硅或锗的纯度。
4. 氢原子光谱:
(1)氢原子光谱线是最早发现并进行研究的光谱线,这些光谱线可用一个统一的公式表示:
![]()
式中:m=1,2,3,…
对每一个m,有n![]() ……构成一个谱线系。
……构成一个谱线系。
![]() (里德伯常数)。
(里德伯常数)。
(2)巴尔末系:巴尔末系是氢光谱在可见光区的谱线,其波长公式:![]()
问题4、对于氢原子光谱的理解问题:
有关氢原子光谱的说法正确的是
A. 氢原子的发射光谱是连续谱
B. 氢原子光谱说明氢原子只发出特定频率的光
C. 氢原子光谱说明氢原子能级是分立的
D. 氢原子光谱的频率与氢原子能级的能量差无关
答案:BC
变式6、
(1)在氢原子光谱中,电子从较高能级跃迁到n=2能级发出的谱线属于巴耳末线系。若一群氢原子自发跃迁时发出的谱线中只有2条属于巴耳末线系,则这群氢原子自发跃迁时最多可发出____________条不同频率的谱线。
答案:6
【模拟试题】(答题时间:45分钟)
*1. 关于α粒子散射实验,下述不正确的是( ).
A. α粒子发生大角度散射的主要原因是原子中有正电荷
B. α粒子发生大角度散射的主要原因是原子中原子核的作用
C. 只有少数α粒子发生大角度散射的原因是原子的全部正电荷和几乎全部质量集中在一个很小的核上
D. 相同条件下,换用原子序数越小的物质做实验,沿同一偏转角散射的α粒子越少
*2. 关于原子的核式结构学说,下述说法正确的是( ).
A. 原子中绝大部分是“空”的,原子核很小
B. 电子在核外绕核旋转的向心力是原子核对它的库仑力
C. 原子的全部正电荷和质量都集中在原子核里
D. 原子核的直径约是![]()
*3. 对α粒子穿过金箔发生大角度偏转的过程,下列说法正确的是( ).
A. α粒子先受到原子核的斥力作用,后受到原子核的引力作用
B. α粒子一直受到原子核的斥力作用
C. α粒子先受到原子核的引力作用,后受到原子核的斥力作用
D. α粒子一直受到库仑斥力,速度一直减小
*4. 如图是α粒子被金原子核散射的径迹,其中不可能的是( ).
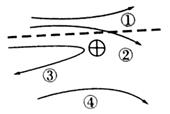
A. 径迹① B. 径迹② C. 径迹③ D. 径迹④
*5. 氕、氘、氚是同位素,则它们( ).
A. 具有相同的质子数 B. 具有相同的中子数
C. 具有相同的核子数 D. 具有相同的化学性质
*6. 物理学家 在研究 时发现电子,这证明 具有复杂结构;以 实验为基础,物理学家 提出原子的核式结构模型,卢瑟福在
轰击 的实验中发现质子,物理学家 在用α粒子轰击铍的实验中发现中子;指出弱相互作用中宇称不守恒的物理学家是 和 ,在实验中证实此结论的物理学家是 .
**7. 氢原子半径是![]() ,根据卢瑟福的原子模型,求:
,根据卢瑟福的原子模型,求:
(1)电子所在轨道的电场强度;
(2)电子绕核运动的速率、频率.
**8. 核磁共振成像(缩写为MRI)是一种人体不接触放射线,对人体无损害,可进行人体多部位检查的医疗影像技术。基本原理是:外来电磁波满足一定条件时,可使处于强磁场中的人体内含量最多的氢原子吸收电磁波的能量,去掉外来电磁波后,吸收了能量的氢原子又把这部分能量以电磁波的形式释放出来,形成核磁共振信号。由于人体各种组织所含氢原子数量不同,或同种组织正常与病变时所含氢原子数量不同,释放的能量亦不同。将这种能量信号通过计算机转换成图像,就可以用来诊断疾病.
(1)关于人体内氢原子吸收的电磁波能量,正确的有( ).
A. 任何频率的电磁波氢原子均可吸收
B. 频率足够高的电磁波氢原子才能吸收
C. 能量大于13.6eV的光子氢原子才能吸收
D. 氢原子只能吸收某些频率的电磁波
(2)人体内吸收了电磁波能量的氢原子( ).
A. 可能处于基态 B. 可能处于激发态
C. 一定电离成氢离子 D. 一定处于激发态
(3)吸收电磁波能量的氢原子释放能量形成的核磁共振信号属于( ).
A. 电信号,是电磁波谱 B. 光信号,是吸收谱
C. 光信号,是连续谱 D. 光信号,是线状谱
![]()
【试题答案】
1. A(原子显电中性,而电子带负电,则原子中一定存在带正电的物质,但是汤姆生的原子模型就不能解释α粒子的散射现象,α粒子大角度散射的主要原因不能直接说是原子中正电荷的作用,而是正电荷集中在原子核中的原因,所以A选项错误,而B选项正确;只有少数α粒子发生大角度散射的结果证明原子存在一个集中所有正电荷和几乎所有质量的很小的原子核,即C选项正确;使α粒子发生大角度散射的原因是受到原子核的库仑斥力,为了使散射实验现象更明显,应采用原子序数大的金箔,若改用原子序数小的物质做实验,α粒子受到原子核的库仑斥力小,发生大角度散射的α粒子少,所以D选项正确. 故题中选不正确的答案是A选项. )
2. A、B (本题考查原子的核式结构学说的内容,由于原子的全部正电荷和几乎全部质量都集中在原子核内,而原子核又很小,所以原子内绝大多数区域是“空”的,A选项正确,C选项是错误的;电子绕原子核的圆周运动是原子核与电子间的库仑引力提供向心力,故B选项正确;原子核的直径约是![]() ,原子的直径约是
,原子的直径约是![]() ,所以D选项错误. )
,所以D选项错误. )
3. B (α粒子被金原子核散射的过程一直受到原子核对α粒子的库仑斥力作用,靠近过程库仑斥力做负功,电子动能减小,电势能增大;远离过程库仑斥力做正功,电子动能增大,电势能减小,在散射过程中电子一直受到库仑斥力作用,电子的速度先减小后增大,即正确选项为B. )
4. B (α粒子被金原子核散射的原因是原子核对α粒子的库仑斥力作用的结果,α粒子靠近金原子核的过程中应由于斥力作用有向外运动的趋势,并且越靠近金原子核,受到的库仑斥力越大,偏转角越大,所以径迹②不可能。故正确选项为B. )
5. A、D (氕、氘、氚的核子数分别为1、2、3,质子数和电子数均为1,中子数等于核子数减去质子数,故中子数分别为0、1、2,互为同位素的原子具有相同的质子数不同的中子数,所以核子数不同,但化学性质由核外电子数决定,而质子数等于中性原子的核外电子数,所以化学性质相同,所以正确的选项为A、D. )
6. 汤姆生 阴极射线 原子 α粒子散射 卢瑟福 α粒子 氮 查德威克 李政道 杨振宁 吴建雄 (物理学是一门以实验为基础的科学,在基础学的发展过程中,物理学家依据不同的实验,提出不同的物理理论,这也是考试出题的一个重要方面,所以要掌握物理学史中与中学物理内容有关的物理学家的理论及其实验基础. )
7. 在卢瑟福的原子核式结构模型中,电子绕原子核做匀速圆周运动的向心力由原子核对电子的库仑力提供.
(1)由点电荷场强公式得
![]()
![]()
(2)由![]() 得
得
![]()
![]()
由![]()
8. (1)D (氢原子只吸收能量等于能级差的光子) (2)B (3)D (氢原子释放能量是以电磁波方式,由于是原子光谱,所以是线状谱、发射光谱.)