![]()
【本讲教育信息】
一. 教学内容:
1. 激光
2. 原子核的组成
3. 放射性元素的衰变
4. 探测射线的仪器和方法
5. 放射性的应用与防护
二. 知识归纳、总结:
(一)激光
1. 自发发射
对于普通的光源,如我们熟悉的白炽灯,灯丝原子吸收了电流做功产生热而被激发到能量较高的状态,由于原子倾向处于能量低的基态,因此处于能量较高状态的原子是不稳定的,会自发地跃迁到较低的能量态,同时放出光子,这就是自发发射(如图所示)。
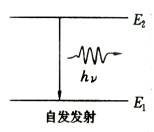
2. 受激吸收
常温下处于热平衡状态的原子系统,多数原子都处在基态,如果一个入射光的能量恰好等于原子基态与某个激发态的能量差,那么原子就很容易吸收这个光子而跃迁到这个激发态上,这种跃迁不是自发产生的,是在入射光子的刺激下产生的,所以称为受激吸收(如图所示)。
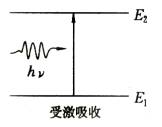
3. 受激发射
如果一个入射光子的能量正好等于原子的某一对能级的能量差E2-E1,那么处于激发态E2的原子就可能受到这个光子的刺激而跃迁到能量较低的状态E1,同时发射一个与入射光子完全相同的光子,这就是受激发射(如图所示)
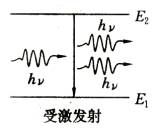
4. 粒子数反转
通常状态下多数原子处于基态,但是如果用一定的手段去激发原子体系,使得在激发态E2上的原子数多于低能态E1上的原子数,这种状态就叫做粒子数反转,是一种非热平衡的状态。
5. 激光产生的机理
对于大多数处于基态的原子,一个入射光子引起的受激发射要比它被吸收的概率大得多,可以形象地说入射光被“放大”了。
但是,受激发射又使处于低能态的原子数增多,受激吸收的效应增强。为了避免这种情况,就需要用抽运装置不断地将回到低能状态的原子再激发到高能态,使上述受激发射的过程不断进行,形成光子的“雪崩”。这样输出的光就是大家都熟悉的激光。
6. 激光器的原理
激光是由激光器产生的.激光器由三部分组成.
(1)激活介质,它能通过受激发射而使入射光放大。
(2)抽运装置,它是使激活介质产生粒子数反转的装置.抽运装置随激光器的类型而异.在固体激光器或染料激光器中采用光抽运,用脉冲光源去照射激活介质;在气体激光器中采用放电激励的手段.
(3)光学共振腔,激活介质放在其中,它能增加放大作用并对发射频率进行选择,如图所示中,反射镜m与半透镜m′,组成光学共振腔.
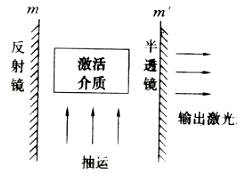
7. 常见的两种激光器
(1)红宝石激光器:以红宝石(A12O3)作为激活介质的激光器,能发出波长为694.3nm的激光.
(2)氦氖激光器:以氦氖为激活介质的激光器最终能输出波长为632.8nm的红色激光.
(二)原子核的组成
1. 天然放射现象
1896年,法国物理学家贝克勒尔发现:铀和含铀的矿物发出一种看不见的射线,这种射线能穿透黑纸而使里面的底片感光,这种现象称为放射性现象,放射性――物质具有发射一些看不见的射线(通过射线与其他物质作用而表现出来)的性质叫放射性,具有放射性的元素叫做放射元素。
2. 对放射线的研究
(1)研究方法:让放射线通过电场或磁场来研究其性质.
把样品放在铅块的窄孔底上,在孔的对面放着照相底片,在没有磁场时,发现在底片上正对孔的位置感光了.若在铅块和底片之间放一对磁极,使磁场方向跟射线方向垂直,结
果在底片上有三个地方感光了,说明在磁场作用下,射线分为三束,表明这些射线中有的带电,有的不带电,如图所示,由三种粒子组成。
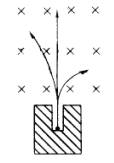
从感光位置知道,带正电的射线偏转较小,这种射线叫![]() 射线;带负电的射线偏转较大,这种射线叫
射线;带负电的射线偏转较大,这种射线叫![]() 射线;不偏转的射线叫
射线;不偏转的射线叫![]() 射线.
射线.
(2)各种射线的性质、特性
<1>α射线:卢瑟福经研究发现,α射线粒子带两个单位正电荷,质量数为4,即α粒子是氦核,其速度是光速的1/10,有较大的动能.
特性:贯穿本领小,但电离作用强,能使沿途的空气电离.
<2>β射线:贝克勒尔证实,β射线是电子流,其速度可达光速的99%.
特征:贯穿本领大,能穿透黑纸,甚至穿透几毫米厚的铝板.但电离作用较弱.
<3>![]() 射线是一种波长很短的电磁波――光子流,是能量很高的电磁波,波长
射线是一种波长很短的电磁波――光子流,是能量很高的电磁波,波长![]() <10-10m。
<10-10m。
特征:贯穿本领最强,能穿透几厘米厚的铅.但电离作用最弱.
3. 质子和中子的发现
(1)质子的发现
<1>1919年,卢瑟福又用![]() 粒子轰击氮,结果从氮核中打出了一种粒子,并测定了它的电荷量与质量,知道它是氢原子核,把它叫做质子(p),后来人们又从其他原子核中打出了质子,故确定质子是原子核的组成部分.
粒子轰击氮,结果从氮核中打出了一种粒子,并测定了它的电荷量与质量,知道它是氢原子核,把它叫做质子(p),后来人们又从其他原子核中打出了质子,故确定质子是原子核的组成部分.
<2>质子带正电荷,电荷量与一个电子所带电荷量相等,质子的质量为mp=1.672623 1×10-27kg.
(2)中子的发现
<1>卢瑟福的预言
1920年卢瑟福提出了一种大胆的猜想:原子核内除了质子外,还存在一种质量与质子的质量大体相等但不带电的粒子,并认为这种不带电的中性粒子是由电子进入质子后形成的.
<2>查德威克发现
查德威克验证了他的老师卢瑟福12年前的预言,原子核中确实存在着中性的、质量几乎与质子相同的粒子,并把它叫做中子(n)。
<3>中子的质量为mn=1.674 928 6×10-27kg.
4. 原子核的组成
原子核是由质子、中子构成的,质子带正电,中子不带电.不同的原子核内质子和中子的个数并不相同.
(1)原子核中的三个整数
<1>核子数:质子和中子质量差别非常微小,二者统称为核子,所以质子数和中子数
之和叫核子数.
<2>电荷数(Z):原子核所带的电荷总是质子电荷的整数倍,通常用这个整数表示原子核的电荷量,叫做原子核的电荷数.
<3>质量数(A):原子核的质量等于核内质子和中子的质量的总和,而质子与中子质量几乎相等,所以原子核的质量几乎等于单个核子质量的整数倍,这个整数叫做原子核的质量数.
(2)原子核中的两个等式
<1>核电荷数=质子数(Z)=元素的原子序数=核外电子数.
<2>质量数(A)=核子数=质子数+中子数.
5. 同位素
原子核内的质子数决定了元素的化学性质,同种元素的质子数相同,核外电子数也相同,所以有相同的化学性质,但它们的中子数可以不同,所以它们的物理性质不同.
定义:具有相同质子数、不同中子数的原子互称同位素.
例如氢的三种同位素:氕(1![]() 、氘
、氘![]() 、氚
、氚![]()
(三)放射性元素的衰变
1. 原子核的衰变
(1)定义:天然放射现象说明原子核具有复杂的结构,原子核放出α粒子或β粒子(并不表明原子核内有α粒子或β粒子,β粒子是电子流,而原子核内不可能有电子存在)后变成新的原子核,这种变化称为原子核的衰变。
(2)衰变规律:原子核衰变时,前后的电荷数和质量数都守恒。
(3)衰变方程:
<1>原子核放出一个α粒子就说它发生了一次α衰变,新核的质量数比原来的核减小了4,而电荷数减小2,用通式表示为:α衰变:![]()
<2>原子核放出一个β粒子就说它发生了一次β衰变,新核的质量数不变,而电荷数增加了1,用通式表示为:β衰变:![]()
<3>![]() 射线经常是伴随α衰变和β衰变而产生,往往是由于衰变后的新核向低能级跃迁时辐射出来的一份能量,原子核放出一个
射线经常是伴随α衰变和β衰变而产生,往往是由于衰变后的新核向低能级跃迁时辐射出来的一份能量,原子核放出一个![]() 光子不会改变它的质量数和电荷数。
光子不会改变它的质量数和电荷数。
(4)两个重要的衰变:![]()
![]()
2. 放射性元素的半衰期
(1)定义:放射性元素的原子核有半数发生衰变的时间叫半衰期。
(2)公式:N余=N原(![]() )t/T m余=m原(
)t/T m余=m原(![]() )t/T
)t/T
式中N原、m原表示衰变前的放射性元素的原子数或质量,N余、m余表示衰变后尚未发生衰变的放射性元素的原子数或质量,t表示衰变时间,T表示半衰期。
(3)确定衰变次数的方法
设放射性元素![]() X经过n次α衰变和m次β衰变后,变成稳定的新元素
X经过n次α衰变和m次β衰变后,变成稳定的新元素![]() Y,则表示该核反应的方程为:
Y,则表示该核反应的方程为:![]()
根据电荷数守恒和质量数守恒可列方程:
![]()
以上两式联立解得:
n=![]()
由此可见,确定衰变次数可归结为解一个二元一次方程组。
(四)探测射线的方法
1. 探测射线的仪器和方法
(1)方法
探测放射线的方法主要是利用放射线粒子与其他物质作用时产生的一些现象来探知放射线的存在,这些现象主要是:
<1>使气体电离,这些离子可使过饱和汽产生云雾或使过热液体产生气泡;
<2>使照相底片感光;
<3>使荧光物质产生荧光.
(2)仪器
<1>威尔逊云室
①构造
云室的主要结构如图所示,圆筒形容器的下底是一个可在小范围活动的活塞;上盖是透明的,通过它可观察云室内发生的现象或进行照相.放射源可放在室内侧壁附近,也可放在室外侧壁的窗口。
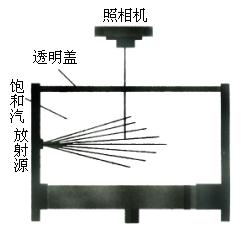
②原理
实验时,在云室内加一些酒精,使室内充满饱和汽.然后使活塞迅速向下移动一段距离,室内气体由于突然膨胀而温度降低,使酒精的饱和汽处于过饱和状态.这时如果有能量较高的粒子从室内气体中飞过,就会使沿途的气体分子电离产生离子,过饱和汽便以这些离子为核心凝成一条雾迹。
③放射线在云室中的径迹
a. α粒子的质量比较大,在气体中飞行时不易改变方向,由于它的电离本领大,沿途产生的离子多,所以它在云室中的径迹直而粗。
b. β粒子的质量小,跟气体分子碰撞时容易改变方向,并且电离本领小,沿途产生的离子少,所以它在云室中的径迹比较细,而且常常弯曲。
c. γ粒子的电离本领很小,在云室中一般看不到它的径迹。
<2>气泡室
气泡室的原理同云室的原理类似,所不同的是气泡室里装的是液体,如液态氢控制气泡室内液体的温度和压强,使温度略低于液体的沸点.当气泡室内压强突然降低时,液体的沸点变低,因此液体过热,粒子通过液体时在它的周围就有气泡形成。
(3)盖革――米勒计数器
<1>构造
计数器的主要部分是计数管,其结构如图所示.
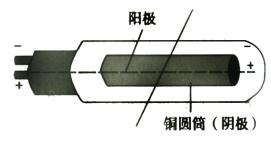
它是一支玻璃管,里面有一个铜圆筒(或在管壁上涂有一层导电薄膜),这是阴极,穿过圆筒轴心的钨丝是阳极.管内充有低压惰性气体,工作时在两极间加上的电压通常略低于管内气体的击穿电压。
<2>原理
当某种射线粒子进入管内时,它使管内的气体电离,产生的电子在电场中被加速,能量越来越大,电子跟管中的气体分子碰撞时,又使气体分子电离,产生电子……这样,一个射线粒子进入管中后可以产生大量电子.这些电子到达阳极,阳离子到达阴极,在外电路中就产生一次脉冲放电,利用电子仪器可以把放电次数记录下来。
<3>优缺点
①优点:放大倍数很大,非常灵敏,用它来检测放射性是很方便的。
②缺点:它对于不同的射线产生的脉冲现象相同,因此只能用来计数,而不能区分射线的种类.如果同时有大量粒子,或两个粒子射来的时间间隔很短(小于200μs)时,也不能计数。
(4)乳胶照相
高速粒子从底片的乳胶层中通过,会使其中的溴化银晶粒电离形成潜像.经显和定影,便可显出粒子的径迹.乳胶照相的优点是可以连续记录,并可得到完整的径迹,便于判断粒子的性质和行为。
2. 核反应
(1)定义:原子核在其他粒子的轰击下生成新原子核的过程,称为核反应.
(2)规律:质量数守恒、电荷数守恒.
(3)几个人工核转变反应方程
<1>卢瑟福发现质子的方程:![]()
<2>查德威克发现中子的方程:![]()
<3>约里奥・居里夫妇发现人工放射性同位素和正电子的方程![]()
3. 放射性同位素及其应用
(1)放射性同位素
天然存在的放射性元素只有四十多种,但用人工方法得到的放射性同位素有一千多种,因而使放射性同位素具有广泛的应用.由于同位素的核电荷数相同,故化学性质相同。
(2)放射性同位素的应用
<1>利用放射性同位素放出的射线(α射线、β射线、![]() 射线)不同的特征去照射物体,达到各种目的。
射线)不同的特征去照射物体,达到各种目的。
①利用放出的![]() 射线检查金属部件是否存在砂眼、裂痕等,即利用
射线检查金属部件是否存在砂眼、裂痕等,即利用![]() 射线进行探伤。
射线进行探伤。
②利用放射线的贯穿本领与物质的厚度和密度的关系,可用它来检查各种产品的厚度和密封容器中的液体的高度等,从而实现自动控制。
③利用放射线使空气电离而把空气变成导电气体,以除去化纤、纺织品上的静电。
④用射线照射植物,引起植物好的变异,也可以利用它杀菌、治病等。
<2>做示踪原子
由于放射性同位素跟同种元素的非放射性同位素具有相同的化学性质,如果在某种元素里掺进一些放射性同位素,那么元素无论走到哪里,它的放射性同位素也经过同样的过程.而放射性元素不断地放出射线,再用仪器探测这些射线,即可知道元素的行踪,这种用途的放射性同位素叫示踪原子.
例如:在给农作物施肥时,在肥料里放一些放射性同位素,这样可以知道农作物在各季节吸收含有哪种元素的肥料.利用示踪原子还可以检查输油管道上的漏油位置,在生物学研究方面,同位素示踪技术也起着十分重要的作用.
(3)放射性的污染和防护
<1>放射性污染
过量的放射性会对环境造成污染,对人类和自然界产生破坏作用.几件需要记住的放射性污染事件是:
①1945年美国向日本的广岛和长崎投了两枚原子弹,当日炸死了十多万人,另有无数的平民受到辐射后患有各种疾病,使无辜的平民痛不欲生.
②1987年前苏联切尔诺贝利核电站的泄露造成了大量人员的伤亡,至今大片土地仍是生物活动的禁区.
③美国在近几年的两次地区冲突(海湾地区、科索沃地区)中大量使用了含有放射性的炸弹,使许多人患有莫名其妙的疾病.
<2>放射性的防护
为了防止有害放射线对人类和自然的破坏,人们采取了有效的防范措施,例如在核电站的核反应堆外层用厚厚的水泥来防止放射线的外泄;用过的核废料要放在很厚很厚的重金属箱内,并埋在深海里,在生活中对那些有可能有放射性的物质要有防范的意识,尽可能远离放射源。
【典型例题】
例1. 如图所示为查德威克实验示意图,由天然放射性元素钋(Po)放出的α射线轰击铍时会产生粒子流A,用粒子流A轰击石蜡时,会打出粒子流B,经研究知道( )
A. A为中子,B为质子 B. A为质子,B为中子
C. A为![]() 射线,B为中子 D. A为中子,B为
射线,B为中子 D. A为中子,B为![]() 射线
射线
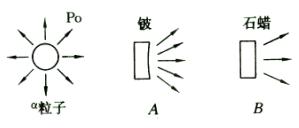
分析:不可见射线A,轰击石蜡时打出的应该是质子,因为质子就是氢核,而石蜡中含有大量氢原子,轰击石蜡的不可见射线应该是中子。
答案:A
例2. 在垂直于纸面的匀强磁场中,有一原来静止的原子核,该核衰变后,放出的带电粒子和反冲核的运动轨迹分别如图中a、b所示,由图可以知( )
A. 该核发生的是α衰变
B. 该核发生的是β衰变
C. 磁场方向一定垂直纸面向里
D. 磁场方向向里还是向外不能判定
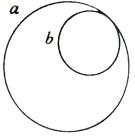
分析:本题考查对α粒子及β粒子的性质的了解,对动量守恒定律以及左手定则的应用能力,原来静止的核,放出粒子后,总动量守恒,所以粒子和反冲核的速度方向一定相反,根据图示,它们在同一磁场中是向同一侧偏转的,由左手定则可知它们必带异种电荷,故应为β衰变;由于不知它们的旋转方向,因而无法判定磁场是向里还是向外,即都有可能。
答案:BD
【模拟试题】(答题时间:30分钟)
1. 关于原子结构和核反应的说法中正确的是( )
A. 卢瑟福在α粒子散射实验的基础上提出了原子的核式结构模型
B. 天然放射性元素在衰变过程中电荷数和质量数守恒,其放射线在磁场中一定不偏转的是γ射线
C. 据图可知,原子核A裂变成原子核B和C要放出核能
D. 据图可知,原子核D和E聚变成原子核F要吸收能量
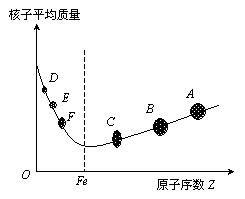
2. 如图所示是原子核的核子平均质量与原子序数Z的关系图像,下列说法正确的是(
)
(1)如D和E结合成F,结合过程一定会吸收核能
(2)如D和E结合成F,结合过程一定会释放核能
(3)如A分裂成B和C,分裂过程一定会吸收核能
(4)如A分裂成B和C,分裂过程一定会释放核能
A.
(1)(4) B.
(2)(4)
C.
(2)(3) D.
(1)(3)
3. 处于激发状态的原子,如果在入射光的电磁场的影响下,引起高能态向低能态跃迁,同时在两个状态之间的能量差以辐射光子的形式发射出去,这种辐射叫做受激辐射,原子发生受激辐射时,发出的光子的频率、发射方向等,都跟入射光子完全一样,这样使光得到加强,这就是激光产生的机理,那么发生受激辐射时,产生激光的原子的总能量En、电子的电势能Ep、电子动能Ek的变化关系是( )
A.
Ep增大、Ek减小、En减小 B. Ep减小、Ek增大、En减小
C.
Ep增大、Ek增大、En增大
D. Ep减小、Ek增大、En不变
4. 太阳的能量来自下面的反应:四个质子(氢核)聚变成一个![]() 粒子,同时发射两个正电子和两个没有静止质量的中微子。已知
粒子,同时发射两个正电子和两个没有静止质量的中微子。已知![]() 粒子的质量为ma,质子的质量为mp,电子的质量为me,用N表示阿伏伽德罗常数,用c表示光速。则太阳上2kg的氢核聚变成
粒子的质量为ma,质子的质量为mp,电子的质量为me,用N表示阿伏伽德罗常数,用c表示光速。则太阳上2kg的氢核聚变成![]() 粒子所放出能量为 (
)
粒子所放出能量为 (
)
A. 125(4mp―ma―2me)Nc2
B. 250(4mp―ma―2me)Nc2
C. 500(4mp―ma―2me)Nc2
D. 1000(4mp―ma―2me)Nc2
5. 一个氘核(![]() )与一个氚核(
)与一个氚核(![]() )发生聚变,产生一个中子和一个新核,并出现质量亏损.聚变过程中( )
)发生聚变,产生一个中子和一个新核,并出现质量亏损.聚变过程中( )
A. 吸收能量,生成的新核是![]()
B. 放出能量,生成的新核是![]()
C. 吸收能量,生成的新核是![]()
D. 放出能量,生成的新核是![]()
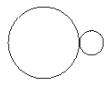
6. 一个原来静止的原子核放出某种粒子后,在磁场中形成如图所示的轨迹,原子核放出的粒子可能是(
)
A. α粒子 B.
β粒子
C. γ粒子 D.
中子
7. 原来静止的原子核![]() ,质量为
,质量为![]() ,处在区域足够大的匀强磁场中,经α衰变变成质量为
,处在区域足够大的匀强磁场中,经α衰变变成质量为![]() 的原子核Y,α粒子的质量为
的原子核Y,α粒子的质量为![]() ,已测得α粒子的速度垂直磁场B,且动能为
,已测得α粒子的速度垂直磁场B,且动能为![]() .假设原子核X衰变时释放的核能全部转化为动能,则下列四个结论中,正确的是( )
.假设原子核X衰变时释放的核能全部转化为动能,则下列四个结论中,正确的是( )
①核Y与α粒子在磁场中运动的周期之比为![]()
②核Y与α粒子在磁场中运动的轨道半径之比为![]()
③此衰变过程中的质量亏损为![]() -
-![]() -
-![]()
④此衰变过程中释放的核能为![]()
A. ①②④ B. ①③④ C. ①②③ D. ②③④
![]()
【试题答案】
1. ABC 2.
B 3.
B 4.
C
5. B 6.
A 7.
D