![]()
������������Ϣ��
һ����ѧ����
�п���һ�ָ�ϰ�������ߵĻ�ѧ���ʣ�����ˮ
���������嵥
1��֪��ˮ����õ��ܼ���
2����ʶˮ�����
3��֪����ˮ���Ȫˮ�����𡢾���ˮ�ķ���
4����ʶˮ�DZ������Ȼ��Դ��ˮ��Ⱦ����Դ��Σ��
5��֪������Ӫ����
6��ѧ�ṹ��ˮ��֪ʶ���硣�˽���ˮ�йص�ʵ��
��
����ȫ��ͻ��
֪ʶ�عˣ�
��һ��ˮ�ķ����뾻����
1������ˮ�ķ��ࣺ
��1������ˮ����ˮ����������
��2����Ȼ���е�ˮ��������Ʒ����Ȫˮ����ɫˮ��ʯ��ˮ�����������
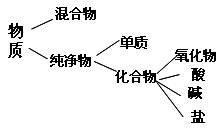
ˮ���ڴ������еĻ�����������е��������������.
2��ˮ�ľ�����
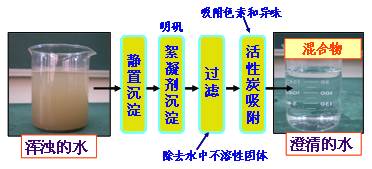
��ˮ��Ӳˮ�ļ�����ת������1�����𣺷���ˮ��������2��ת������С�����
������ˮ����ɺ��ɣ�
1��ˮ����ɣ�
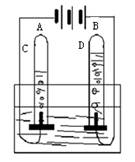
1��ʵ��������
�Թ�������ɫ����ð������Դ�������������Թ��в������������Ϊ1��2
2����������ʲô�����������֤��
�����������ǵ�ľ��
��������ȼ����һ�����ձ�
3����ѧ����ʽ��
2H2O![]() 2H2��+ O2 ��
2H2��+ O2 ��
4��ʵ�������Ԫ��֪ʶ��
ˮ������Ԫ�غ���Ԫ�����
��ѧ�仯��ʵ�ʣ����ӷ�Ϊԭ�ӣ�ԭ��������ϳ��·���
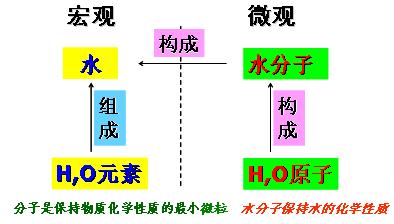
2����H2O���ĺ��壺��ʾ��1��ˮ��2��ˮ������Ԫ�غ���Ԫ����ɵģ�3��һ��ˮ���ӣ�4��һ��ˮ������2����ԭ�Ӻ�1����ԭ�ӹ��ɡ�
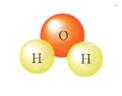
������ˮ��Ӧ�ã�
1��ˮ�����
2��ˮ��������Ҫ��6��Ӫ����֮һ�����ˮ�ģȺͣ�Ԫ�ض�������ij���Ԫ��
3��ʵ���е�ˮ��
��1������ʵ�������
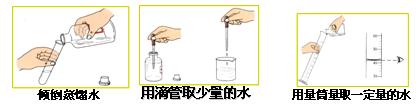
��2��ˮ�ĵ��
��3�����ˡ�������������Һ
��4����������
��5��ˮ��ʵ���е���;��
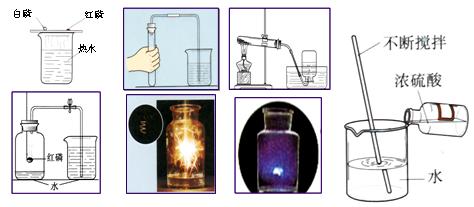
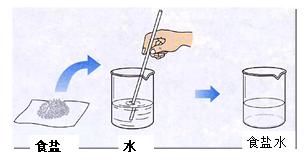
����ˮ�ų��������ȵ����� ������ˮ���մ������ȵ�����
��ˮ��Ӧ�ų��������ȵ�����
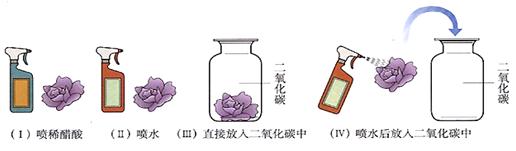
��6��̽������ȼ�պ�IJ��
��7������������Ŀ����ͺ����������̽��
��8��������̼�����ʣ�
4��ˮ����Ҫ����Դ
��1��ˮ��Ⱦ��Σ����
Ӱ�칤��ũ����ҵ���������ƻ�ˮ����̬ϵͳ������ֱ��Σ�����彡����
��2������ˮ��Դ����ֹˮ����Ⱦ������ҵ��ũҵ��������ˮ������Լ��ˮ.
���ģ���ˮ�йصĻ�ѧ��Ӧ
1����ˮ�μӵĻ�ѧ��Ӧ��
��1���ֽⷴӦ��ˮ���
��2�����Ϸ�Ӧ����ʯ����ˮ����Ӧ����Һ�ʼ��ԣ�pHֵ����7��
������̼��ˮ ����Ӧ����Һ�����ԣ�pHֵС��7��
2��д����ˮ���ɵķ�Ӧ
��1�����Ϸ�Ӧ������ȼ��
��2���ֽⷴӦ������������ֽ� ��̼��ֽ�
��3���û���Ӧ��������ԭ����ͭ
��4�����ֽⷴӦ����������������� ������� ��̼���κ���
��5��������Ӧ������Һ��ǽ���������
���壩ˮ�ļ�������գ�
1��ˮ�ļ��飺����ˮ����ͭ������ˮ����ͭ�ɰ�ɫ��Ϊ��ɫ��˵����ˮ���ڣ�
CuSO4+5H2O=CuSO4��5H2O
2��ˮ�����գ�����Ũ���ᡢ��ʯ�ҡ������������ơ�����
���������⡿
��1�����й���ˮ��������ȷ���ǣ��� ����
A��ˮ��û����ζ��û��ζ���ĵ���ɫ��Һ��
B��ˮ���ܶ���1��/cm3
C��
D��ˮ�ķе���
E��ˮ�������������ɫ����
F����
G��ˮ����ȼ��
H����Ȼ���е�ˮһ�㶼��������
I��������ˮ�ǵ���
������������ˮ���������ʡ���ѧ���ʼ�����
���𰸡�E F G H
��2����Ұ��������������м������轫��ˮת��������ˮ������ѧ��������������������ɱ����Ư�ۣ�����Ȼ������������С����ϴ��������������˳���ǣ� ��
A. �ۢڢ٢� B. �ۢ٢ڢ� C. �ۢ٢ܢ� D. �٢ۢڢ�
���������ɰ�����ˮ���ľ�ˮ����ˮ
���𰸡�B
��3��ˮ������֮Դ������ˮ��Դ����ֹˮ��Ⱦ��ÿ�������ȫ��������.�������������ڷ�ֹˮ��Դ��Ⱦ���ǣ� ��
��ũҵ������Ҫ����ʩ��ũҩ�ͻ��� ����ҵ��ˮ��������ˮ�����������ŷ�
�����ú���ϴ�·�
������ˮ����
A. �٢ڢ� B. �ڢۢ� C.�٢ڢ� D. �٢ڢۢ�
��������ˮ����Ⱦ��Ҫ�ɹ�ҵ��ũҵ������ȷ�����ɡ�
���𰸡�C
��4�������ǵĺ�ˮ����ͼ��ʾ�ļ���ˮ�����о��������л���̿��������_____���ô�װ�þ�����õ���ˮ����_____���������������������������������Ϊ��������ˮ���������������������������� ��Ӳˮ�����ˮ��
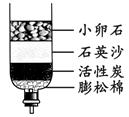
������������̿����Ҫ�����������ж�����ɫ��������ζ�������ʡ����ܽ�ˮת��Ϊ���������ˮ��
���𰸡����� ����� ������
��5��������Ӿ��������ˮ��������������Դ��һ��������������������������ˮ���������������ˮ�����������й���ˮ���ӵ�˵����ȷ���ǣ� ��
A. ˮ�����Ǽ�С��ˮ��
B. 1��ˮ������1������Ӻ�1����ԭ�ӹ���
C. 1��ˮ������2����ԭ�Ӻ�1����ԭ�ӹ���
D. ˮ���Ӳ����ٷ�
�����������飺��1�����ӵ����ʣ�2��������ԭ�ӹ���
���𰸡�C
��6����ˮ�����Ĺ����У�����˵����ȷ����____ _ ������ĸ����ѡ�⣩
A. ˮ���Ӳ����˶�
B. ˮ����֮��������
C. �⡢��ԭ�Ӳ������ı� D. ˮ���ӿ��Ա���ˮ����������
��������ˮ�����������仯�������仯�з��ӱ������䣬�ı���Ƿ��Ӽ�ļ�����˶����ʡ�
�ɷ��ӹ��ɵ����ʣ��仯ѧ�����ɷ��ӱ��֡����������ɷ��ӵľۼ��������
���𰸡�A C
��7��ͼ1Ϊ���ˮ����������ʱ���ϵͼ��ͼ2�ǵ��ˮ�ļ���װ�á��Իش��������⣺
��1�������Թ���������A�����Ӧ���ӵ�Դ�� ��
��2��0s��3s��������Թ���������������8sʱ�������Թ�������������
��������ͬ��������ͬ��������һ���������ԭ�������
����1�㼴�ɣ�
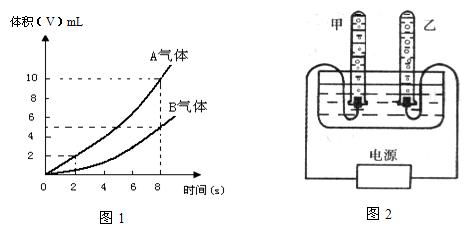
����������ס���ӵ�Դ�����������Թ��в�������������ơ���ϵѧ����������������֪ʶ
���𰸡���1������2����ͬ
�������ܽ��Ա�����ǿ
��8����ͼ�dz��л�ѧ�г������ʼ��ת����ϵ�����мס��ҡ�����Ϊ�ǽ������ʣ�A��B��E�Ͷ���Ϊ�����B��EΪ�ܲ�������ЧӦ�����塣
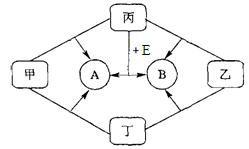
��1��д����ѧʽ��
��
����
��2��д������E��Ӧ����A��B�Ļ�ѧ����ʽ
��3��D��A�����Ԫ����ͬ�Ļ����д��D��MnO2�������������£��ֽ�����A�ͱ��Ļ�ѧ����ʽ��
��������ͨ��ȫ����ҳ�ͻ�ƿڡ�������B��EΪ�ܲ�������ЧӦ���������뵽����ѧ���Ķ�����̼�ͼ��飬������ѧ���Ļ�ѧ��Ӧ�����ƶϡ�
���𰸡���1��H![]() CO2 + 2H2O
CO2 + 2H2O
��3��2H2O2 ![]() 2H2O+ O2 ��
2H2O+ O2 ��
��9����ˮ�峺�����������ʣ���Ӳˮ���϶�����Ըƺ�þ�Ļ����������ƿ��ɫҺ�壬�ֱ�Ϊ��ˮ��Ӳˮ���������С��ͬѧ��ˮ��̽�������ش��й����⣺
���������������������˺�����ȷ����ɾ���ˮ�������ܽ���ˮ��Ӳ�ȵ���
��
������ˮ��Ӳˮ�ķ����ж��֡�С�����õķ����ǣ��ֱ�ȡ�����������У��������ɣ��й�����������Ӳˮ�����������һ�ַ������������衢����ͽ��ۣ���
��С������ʵ��ʱ������Ӳˮ�������Ĺ����У��������������岢�õ�һ�������ԵĹ��塣
�������������������������Ƕ�����̼�������Թ��������̼���Ρ�
�����ʵ����
�������ɵ�����ͨ�� �У��۲쵽
������֤�������������Ƕ�����̼��д���йط�Ӧ�Ļ�ѧ����ʽ
��
�������������ԵĹ����е���
���۲쵽�д������ݲ����������ֹ��������̼���Σ������ֹ�����̼��ƣ�д���÷�Ӧ�Ļ�ѧ����ʽ��
��
��������Ӧ����ͨ������ʵ��õ��������ڼ������ ��ȥ��ˮƿ���ڱ��ϵ�ˮ����
�������������г�����з�����ˮ��Ӳ�ȣ�ʵ�����ﳣ������ʹӲˮ����������Ӳˮ����ˮ�ij��÷����У����������ɷ����й�����������Ӳˮ������������Ϊ��ˮ����������ˮ�ֱ���뵽ʢ����ˮ��Ӳˮ���ձ��У����裬����������ĭ������ˮ��������ĭ��������û����ĭ����Ӳˮ�������л�����������̼��ʹ�����ʯ��ˮ����ǣ���Ӧ����ʽΪ��CO2 + Ca��OH��2 ===
CaCO3��+ H2O��̼������������Һ�������ֽⷴӦ���йط�Ӧ����ʽΪ��CaCO3 + 2HCl === CaCl2
+ H2O + CO2����
���𰸡������� ���ֱ�ȡ�����ձ��У�������������ˮ�����裬������ĭ�϶���Ǵ�ˮ������ĭ����ĭ���ٵ���Ӳˮ �Ǣ������ʯ��ˮ������ʯ��ˮ����ǣ�
CO2
+ Ca��OH��2 === CaCO3��+
H2O
��ϡ����ȣ�CaCO3 + 2HCl === CaCl2 +
H2O + CO2����ʳ�ס�
�ġ�����С��
����ˮ��֪ʶ��Ҫ�����˽̰������ѧ�ϲ�ĵ�����Ԫѧϰ��.�����漰����ˮ����ɵIJⶨ��ˮ�ľ�����Ӳˮ����ˮ��ˮ��Դ�ı��������ϡ�������������ˮ�йص�֪ʶҲ�ر�࣬��������к���ˮ��������������ʴҲ��ˮ�йأ�����Ӫ������Ҳ��ˮ��ˮ��������ܼ��������ᡢ��ε�ѧϰ�У��ܶ�ķ�ӦҲ������ˮ��Һ�н��еģ����Һܶ���Ҫ�ķ�ӦҲ����ˮ���ɡ���Щ����Ӧ�ܷⱣ��Ҳ��ˮ�йء�����ˮ��Ϊһ����������ʣ�ͬʱҲ�Ǻ���Ҫ�ġ�
�塢Ӧ������
��ר���������ߵĻ�ѧ���ʲ��֡��Ե������ʡ���ˮΪ�����Ѷ����Ԫ���ص�֪ʶ�ͼ�����ϵ��һ�𣬹�����һ�����������֪ʶ��ϵ����ר����ѧ����ѧϰ������������ѧ�Ļ����Ͻ��е�֪ʶ��˼ά���������ۺ�ѵ��ר�⡣��ʵ�ñ�ר������ݻ�Ϊ�Ժ���ۺ�ѧϰ���¼�ʵ�Ļ�����
������ǰ˼ά����̼��̼�������
1��̼��
��1������̿��ľ̿����ǿ�ҵ�
�ԣ����������� ���ʡ�
��2����ѧ���ʣ�
����ȼ����
��ȫȼ��������������������CO2����ѧ����ʽ
�� ��Ӧ��
����ȫȼ����������������������CO����ѧ����ʽ
�� ��Ӧ��
����ԭ�ԣ�ľ̿��ԭ����ͭ����ѧ����ʽ
�� ��Ӧ��
ʵ������
ľ̿��ԭ����������ѧ����ʽ
�� ��Ӧ��
2��������̼��
��ѧʽ
��Է������� ��Ԫ��֮���������
���ֶ�����̼�Ļ�ѧ���ʵ���С������
��1���������ʣ� ɫ�� ζ���������ܶȱȿ��� �� ����ˮ����ѹ�����¿ɵù��������ɱ�
��2����ѧ������
��һ������²���ȼ����Ҳ��֧��ȼ�գ����ܹ�������
����ˮ��Ӧ����̼�
�� ���ɵ�̼����ʹ��ɫ��ʯ����Һ��죬̼��ȶ����ֽ�
����ʹ�����ʯ��ˮ����ǣ�
����Ӧ�����ڼ��������̼!
��3��ʵ������ȡ�����˼·����ԭ����װ�á����飩
������װ�ã���
�� ������
���ռ���������
��
������
��4��������̼��ʵ�����Ʒ�
��ԭ������ʯ��ʯ��ϡ���ᷴӦ��
��ѡ�ú�
��ͬ�ķ���װ��
�������ռ�������
����֤������
���Ƕ�����̼��
������������
֤���Ѽ���������̼���塣
��5��������̼�Ĺ�ҵ�Ʒ���
����ʯ��ʯ��
��ʯ�Һ�ˮ��Ӧ�ɵ���ʯ�ң�
��6����;������������ԭ����Na2CO3+2HCl=2NaCl+H2O+CO2�������������������ʣ��������仯ѧ���� ���ɱ������˹����ꡢ����������ҷ���
������̼����Ի�����Ӱ�죺�ŷŹ�������
ЧӦ��
��7���ж�����̼���ɵķ�Ӧ����̼�ڿ����г��ȼ��
����̼��������顢�Ҵ��ȣ�ȼ��
����������ʯ��ʯ
��ʵ�����ƶ�����̼
������̼���κ�����Һ�ķ�Ӧ
�磺̼���ƺ�ϡ����
̼�����ƺ�ϡ����
��CO��ԭ������
3��һ����̼��
��ѧʽ
����Է�������
����Ԫ��֮���������
��1���������ʣ���ɫ����ζ�����壬�ܶȱȿ�����С��
����ˮ
��2���ж�������������ѪҺ�е�
��ϣ�ʹ����ȱ���������ж���
��3����ѧ��������H2��CO��C�������ƵĻ�ѧ���ʣ�����ȼ�� ����ԭ����
����ȼ�ԣ�
����ȼǰһ��Ҫ����
��
����ԭ�ԣ���ҵ����
������
ɫ��ĩ��� ɫ��ʯ��ˮ��
����
��ģ�����⡿������ʱ�䣺40���ӣ�
1. ���м�ͥ��ˮϰ���У�����Ϊ�������ǣ�
A. ϴ����ϴ��ʱ��ˮ������ֹ
B. ϴ�֡�ϴ����ˢ��ʱ����ʱ�ر�ˮ��ͷ
C. ϴ���ʱ����ϳ�ϴ
D. ϴ�ˡ����ס�ϴ�µ�ˮ�����������ϵء������
2. ��Ӳˮϴ�·������˷ѷ�������ϴ���ɾ���������ҪʹӲˮ�������ɲ��õķ����ǣ�
A. ���� B. ��� C. ���� D. ����
3. ijͬѧ���˺�����ɳ��ˮ����Һ��Ȼ���ǣ���ԭ������ǣ�
A. ��ֽ��©��֮��������
B. �㵹Һ��ʱҺ�������ֽ��Ե
C. ����ʱ����������������ֽ��һ��
D. ©�����¶�û�п����ձ�����
4. ˮ��һ����Ҫ����Ȼ��Դ�����������桢��ũҵ������ϢϢ��أ����¹���ˮ��˵������ȷ���ǣ�
A. ���������3/4�����������ˮ�����ˮ��ȡ֮������֮���ߵ���Ȼ��Դ�����ر���ˮ��Դ
B. ˮ���ܶȱȱ����ܶ�С������ˮ�������ܰ�ȫԽ������Ҫ��֤
C. ˮ�ı��ȱ�ɰʯ���������Ĵ�ö࣬�����غ�������ҹ�²����½С����Ҫԭ��
D. ������Ȫˮ�в����κλ�ѧ����
5. ����˵������ȷ���ǣ�
A. ����̿����Ӳˮת������ˮ B. ��¯��ˮӲ��̫��ʮ��Σ��
C. ����ˮ�Ǿ����̶Ƚϸߵ�ˮ
D. ���˲������Գ�ȥˮ�е�������
6. ��������Ԫ�صĴ�����ˮ�����ŷ��������ˮ��ͽ����������ˮ�����ೱ��ˮ����Ⱦ���⡣���������У�����ʹ�ò�������ˮ�����ೱ���ǣ�
A. CO��NH2��2 B. Ca��H2PO4��2
C. Na2CO3 D. Na5P3O10
7. ��ͼ��ˮ������һ�������·ֽ��ʾ��ͼ�����л�õ���Ϣ����ȷ���ǣ�
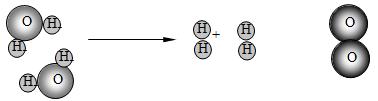
A. һ��ˮ������������ԭ�Ӻ�һ����ԭ�ӹ���
B. ˮ�ֽ�����������������ķ�����֮��Ϊ2��1
C. ˮ�ֽ�����У����ӵ������
D. ˮ�ֽ�����У�ԭ�ӵ���Ŀ���䡣
8. ����ѧ����־����2004��ʮ��Ƽ�ͻ�ƣ���������������������ˮ��Ӱ����������һ����һ�Ƽ�ͻ�������й���ˮ��˵����ϵ�����е��ǣ�
A. ˮ�ǻ�����
B. ˮ���ʱ��������������
C. ˮ�й̡�Һ��������״̬ D. ������������άϵ��Ҫˮ
9. �ճ����������dz��ȴ���ˮ���г��ϳ��۵Ĵ���ˮ��һЩ������ˮ��������һ�ി��ˮ������˵���У���ȷ���ǣ�
A. ����������ǿ
B. ����pH������
C. ��������������Ŀ����ʵȶ�����Ԫ��
D. ����ࡢ���������������öԽ�������
10. ��ˮ���¶Ⱥ�ѹǿ���ߵ��ٽ�㣨t =
A. ���ٽ�ˮ�ɴ����ж��� B. ���ٽ�ˮ��һ��������
C. ���ٽ�ˮ��ˮ��һ��״̬ D. ���ٽ�ˮ�����������γɶ�����Ⱦ
11. ��Ȼ�������ֳ���ʽ�ṩ����Դ��Ϊһ����Դ��������������Դ�����������ȡ����Դ��Ϊ������Դ������������Ч������Ⱦ�Ķ�����Դ��������ˮ�ƶ�����Դ�����������о�������ȷ���ǣ�
A. ����ˮ����������ǿ�ȼ�յ����ʣ���˿��о��ڲ��ֽ������£�ʹ���Ϊ������Դ
B. �跨��̫���ܾ۽����������£�ʹˮ�ֽ��������
C. Ѱ�Ҹ�Ч������ʹˮ�ֽ����������ͬʱ�ͷ���Դ
D. Ѱ�����⻯ѧ���ʣ����ڿ���������Դ���Էֽ�ˮ��ȡ����
12. �����벻��ˮ������ˮ��֪ʶ���ճ����������Ź㷺��Ӧ�ã�
���豭�ڵ�ɴ�����ɽ���Ҷ���ˮ���룬�������ã���������õĻ�ѧԭ���� ��
�����ƾ�ˮ���г�����
�����ڳ�ȥˮ�е���ζ��ɫ�ء�
������ˮ���ö�����������ɱ�����������ȵĻ�ѧʽΪ ��
����ˮ�к��н϶�ĸơ�þ���ӣ�Ϊ����Ӳ�ȣ��ɲ��õķ�����
13. ��Ȫˮ���ÿ�Ȫˮ����Ӳˮ��������ˮ���״ס��ƾ����dz�������ɫҺ�壬���ǵ���۷dz����ƣ����о�����ζ����
�� ���������ǿ���ѡ�õĻ�ѧ������
��ֻ��һ�֣�������������ɫҺ����ö��ַ������֡����磺
������
������ţ������ݲ�����ĭ�Ķ��������֣�
������ˮ ������̿
��ʳ��ˮ
������������ɫҺ��ֱ���ȣ���ȫ�����������Ƿ��� �������������֡�
14. ij���ںӺ�����Ư��������㡣С����Ѷ��ȡ��ˮ����ͬѧ��һ��̽����
���۲�ˮ�ʵ��ܼ��ȣ�Ȼ����ˣ�����ʱ�����õ����������е�
������ű�ʾ����
A. ©�� B. �ձ� C. ������ D. ����̨ E. �ƾ���
��ȡ���˺��ˮ���������ֲ�ͬ���͵�����������ˮ���Ƿ������ԣ�����ѡ�õ����ʿ�����
��
������ѡ�������������е�һ�֣����һ��ʵ�������֤
|
ʵ����� |
ʵ������ |
ʵ����� |
|
|
|
|
15. ��ij�ε��ˮ��ʵ���м�����������NaOH��Һ���ֲ�÷ֱ����Դ�������������������������ϲ����������ʵ���������£�
|
ʱ�䣨���ӣ� |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
�����������������cm3�� |
6 |
12 |
20 |
29 |
39 |
49 |
55 |
65 |
75 |
85 |
|
�����������������cm3�� |
2 |
4 |
7 |
11 |
16 |
21 |
26 |
31 |
36 |
41 |
����ϸ��������ʵ�����ݣ�1 ~ 6�������������������ɵ��������֮�ȴ���2��1�����ܵ�ԭ����
���ӵ�7���ӿ�ʼ��ÿ�������������������������֮��ԼΪ2��1�����ܵ�ԭ����
��
������������Ϊ5%��NaOH��Һ
16. ʵ��ⶨ��Ӳˮ�к��н϶�Ŀ����Եĸơ�þ�Ļ�������иƵĻ�����ΪCa��HCO3��2�������ֽ⡣�����������ˮ�ʹ������壬����һ�������Ե��Σ�������ˮ���ijɷ�֮һ��
��1�������������̽��Ca��HCO3��2���ȷֽ���������������
��2������������С����Ϊ�������е���������Ƕ�����̼��
������Ϊ�������еĹ��������
��
��3�������ʵ�鷽����������Ƴ���ʵ�鷽������֤���������Ƿ���ȷ��
��4������������������С���IJ�����ȷ������Ӧ����
��
�����IJ�����ȷ������Ӧ����
��
��5��д��Ca��HCO3��2���ȷֽ�Ļ�ѧ����ʽ
��
![]()
������𰸡�
1. D 2. B 3. B 4. C 5. B 6. C 7. C 8. D 9. D 10. B 11. A
12. ������ ������̿ ��ClO2
����������������
13. �״� �ƾ� ����һ�����Թ��ڷֱ��������������Һ�������м�����ɫʯ����Һ�����ֱ��������ǰ״ף���������������������Һ�����������У��ܵ�ȼ���Ǿƾ����� �� ��������
14. ��
E ����ɫʯ����Һ ��Na2CO3��Һ��
ʵ�������ȡ����ˮ�����Թ��У��μӼ�����ɫʯ����Һ����μ�Na2CO3��Һ����
ʵ��������ɫʯ����Һ��죨�������ݲ����� ʵ����ۣ�ˮ�������ԡ�
15. ���������𰸡��� ������������ˮ�е��ܽ����������ǰ6���ӣ��������������ɵ��������֮�ȴ���2��1����7���Ӻ�������ˮ�е��ܽ�ﵽ���ͣ�����������������������֮��ԼΪ2��1��
�� ���ˮ�Ĺ����У������������ʵ��������ı䣬�������ˮ������Ϊ��
16. ���������𰸡��� ̼��ƣ�CaCO3 �� �� �������ɵ�����ͨ������ʯ��ˮ�� �� �����ɵĹ����еμ�ϡ���� �� �����ʯ��ˮ����ǣ������ܽ������ɫ���塣
��5��Ca(HCO3)2
= CaCO3 + H2O + CO2��