![]()
������������Ϣ��
һ����ѧ����
��ѧʽ�뻯�ϼ�
���������嵥
1���˽⻯ѧʽ�ĺ���
2��֪��һЩ����Ԫ�صĻ��ϼۺ�ԭ���ŵĻ��ϼ�
3�����û�ѧʽ��ʾijЩ���ʵ���ɣ��������û��ϼ�����ѧʽ
����ȫ��ͻ��
֪ʶ��1����ѧʽ



![]()
ˮ
ˮ���ӵľۼ�
ˮ���� ��ѧʽ
һ����Ԫ�ط��ű�ʾ������ɵ�ʽ�ӽ�����ѧʽ��

������ѧʽ������
��1���ɷ��ӹ��ɵ������仯ѧʽ������
|
���� |
���� |
ʵ�� |
|
��� |
�ٱ�ʾһ������ |
ˮ |
|
�ڱ�ʾ���ʵ����Ԫ�� |
ˮ����H��O����Ԫ����ɵ� |
|
|
�� |
�ٱ�ʾ���ʵ�һ�����ӣ���ԭ�ӣ� |
һ��ˮ���� |
|
�ڱ�ʾ���ʵķ��ӹ��� |
ÿ��ˮ��������2����ԭ�Ӻ�1����ԭ�ӹ��ɵ� |
ע�⣺��ѧʽǰһ�������֣��Ͳ��ܱ�ʾ���ʺ����Ԫ�أ�ʧȥ�˺�����壬ֻ���������塣
������3H2O �ߣߣߣߣߣ�
��2H2O�и�������ʲô���壿
���ֵ�����
|
���� |
���� |
ʵ�� |
|
ǰ�� |
�ٱ�ʾ�������ʵķ��ӣ���ԭ�ӣ�����Ŀ |
2��ˮ���� |
|
�� |
�ڱ�ʾ�������ʵķ�����ij��ԭ�ӵ���Ŀ |
ÿ��ˮ��������2����ԭ�� |
��2����ԭ�ӹ��ɵ����ʣ��仯ѧʽ������
��ۣ��ٱ�ʾ����
�ڱ�ʾ��ɸ����ʵ�Ԫ��
�ۣ���ʾһ��ԭ��
���������⡿
��1��O2��ʾ�����������Ա�ʾ������Ԫ�أ���һ�������ӣ���������Ԫ�أ�����������Ԫ����ɣ���ÿһ����������������ԭ�ӹ��ɣ���������ԭ�ӡ���ȷ����
A. �٢ڢ� B. �ڢܢ� C. �ڢܢ� D. �٢ܢ�
����������ѧʽ�����������㣺�ٱ�ʾһ�����ʣ���O2��ʾ�������ڱ�ʾ���ʵ�һ�����ӣ���O2��ʾһ�������ӣ��۱�ʾ������ʵĸ���Ԫ�أ���O2����Ԫ����ɣ��ܱ�ʾ����һ�������и�Ԫ�ص�ԭ�Ӹ�������O2��ʾһ����������������ԭ�ӹ��ɣ��ݱ�ʾ������ʸ�Ԫ�ص������ȣ��ޱ�ʾ������ijԪ�ص��������������⣬��Ҫ����Ԫ�غ�ԭ�ӵĸ����Ԫ��ֻ������۸��������Ǵ���ģ���������ԭ��Ӧ��ʾΪ2O��
���𰸡�B
��2��д�����з�������ʾ�����壺
��1��H________ ��2��2H________ ��3��H2________ ��4��2H2________
��������������ؼ���Ҫ����Ԫ�ط��ż���ѧʽ���壬Ū��Ԫ�ط�����Χ��ͬλ���ϵ���������ʾ������.
���𰸡�
��1��H����ʾ��Ԫ�أ���ʾһ����ԭ��.
��2��2H����ʾ2����ԭ��.
��3��H2����ʾ��������ʾ����������Ԫ����ɣ���ʾһ������ӣ���ʾ1������Ӻ���2����ԭ��.
��4��2H2��ʾ2�������.
֪ʶ��2�����ϼۣ�
|
�������� |
�Ȼ��� |
�Ȼ�þ |
�Ȼ��� |
|
��ɱ�ʾ |
NaCl |
MgCl2 |
AlCl3 |
|
�������� |
�Ȼ��� |
ˮ |
���� |
|
��ɱ�ʾ |
HCl |
H2O |
NH3 |
һ��Ԫ�ػ��ϼ۵ı�ʾ������
���ϼ���+1��+2��+3����1����2������ʾ������Ԫ�ط��ŵ����Ϸ���Ҫע�⻯�ϼ۵ı�ʾ���������ӷ��ŵ���������������ɷ�����+��2+������2��������ʾ������Ԫ�ط��ŵ����Ͻǣ��磺Na+��Cl����Mg2+��O2����
������![]() ��Ca2+��
��Ca2+��![]() ��S2�������ֵĺ��塣
��S2�������ֵĺ��塣
![]() ��ʾ��Ԫ����+2�ۣ����Ԫ�صĻ��ϼ�Ϊ+2�ۣ���
��ʾ��Ԫ����+2�ۣ����Ԫ�صĻ��ϼ�Ϊ+2�ۣ���![]() ��ʾ��Ԫ������2�ۡ�
��ʾ��Ԫ������2�ۡ�
Ca2+��ʾһ�������Ӵ�2����λ������ɣ�S2����ʾ1�������Ӵ�2����λ�ĸ���ɡ�
����Ԫ�ػ��ϼ۵�һ����ɣ�
��1����Ԫ�صĻ��ϼ�ͨ����+1�ۣ���Ԫ�صĻ��ϼ�����2�ۡ�
��2���ڻ������У�����Ԫ��Ϊ���ۡ�
��3���ǽ���������������ʱ���ǽ���Ԫ���Ը��ۣ��ǽ�������Ԫ�ػ���ʱ���ǽ���Ԫ�������ۡ�
Ԫ���ڲ�ͬ������ͬ���������п��Բ�ͬ�Ļ��ϼۡ�
��4���ڻ������У����������ϼ۵Ĵ�����Ϊ�㡣
��5�����ϼ���Ԫ�����γɻ�����ʱ�����ֳ���һ�����ʣ���ô�ڵ����Ԫ�صĻ��ϼ�Ϊ0��
�����μdz���Ԫ�ؼ�ԭ���ŵĻ��ϼ�
1������Ԫ�صĻ��ϼ�
|
+1 |
�ء��ơ��⡢�� |
+2 |
����þ���ơ�п��ͭ |
|
+3 |
�� |
��1 |
�� |
|
��2 |
�� |
+2��+3 |
�� |
2������ԭ���ŵĻ��ϼ�
|
�������� |
笠� |
������ |
����� |
����� |
̼��� |
|
���ӷ��� |
NH4+ |
OH�� |
NO3�� |
SO42�� |
CO32�� |
|
���ϼ� |
+1 |
��1 |
��1 |
��2 |
��2 |
�ģ����ϼ۵�Ӧ����
1����д������Ļ�ѧʽ��

A�����䣺���ʻ�ѧʽ����д������
��1�����

��2��������һ���Ԫ�����ơ����塰Ԫ������+����
B. ������Ļ�ѧʽ������д˳���෴��д���� H�� O��
��1����д���裺��д����ɻ������Ԫ�ط���
����Ԫ����ǰ���ǽ���Ԫ���ں�����Ԫ����ǰ������Ԫ���ں�
�ڱ��Ԫ�صĻ��ϼ�
��ʮ�ֽ��棨����ֵ��
��ȡ��С��Լ����ʡ������1
�ݼ�黯ѧʽ ��������Ԫ�ػ��ϼ۴�����Ϊ�㡣
����������
��2��������
������Ԫ����ɵĻ����������
����Ԫ�ص����ƣ��������������ij��ij����
��NaCl�������Ȼ��ơ���ZnO����������п����Fe3O4����������������������Ҫע�⣬H2O���ǡ�ˮ�������ܶ��ɡ������⡱��NH3���ǡ���������
�ǽ���������һ���������������ij��
��OH��β�Ļ������������ԭ���Ÿ������ڡ�1��ʱ�������ű�ʾ��ֻ��һ��ԭ����ʱ�����ؼ����ţ�
һ������Ϊ��������ij���磺NaOH�������������ơ���Cu��OH��2������������ͭ��
���������笠��������������ԭ���ţ���β�Ļ����������
������������笠���+���
һ�����ԭ���ź���һԪ�ص����ƴ��ҵ����˳�������ij��ij����
�磺CaCO3������̼��ơ���Cu��NO3��2����������ͭ��
����H+���������ij�ᡱ��H2CO3�Ͷ�����̼�ᡱ��H2SO4�Ͷ��������ᡱ�ȡ�
2�����ݻ�ѧʽ��δ֪Ԫ�صĻ��ϼ�
�����������л��ϼ۴�����Ϊ�����δ֪Ԫ�صĻ��ϼ�
����H2SO4
3���жϻ�ѧʽ����д�Ƿ���ȷ
�����������л��ϼ۴�����Ϊ��
����MgCl
���������⡿
��1��д���������ʵĻ�ѧʽ��
��1������ ��2������ ��3����� ��4��ͭ ��5�������� ��6������������ ��7���Ȼ��� ��8���Ȼ���
����������д���ʵĻ�ѧʽ��Ҫ�������¹涨��
��1���ɵ�ԭ�ӹ��ɵ����ʣ�ͨ������Ԫ�ط��ű�ʾ���ǵĻ�ѧʽ����Ne��
��2���������ʺ�̬�ǽ������ʣ����ڽṹ���ӣ�ϰ������Ԫ�ط��ű�ʾ����S��Cu��
��3��˫ԭ�ӵ��ʵķ��ӣ�����д����ɵ��ʵ�Ԫ�ط��ţ�Ȼ����Ԫ�ط��ŵ����½ǣ�д��һ��С��2������N2��
��4����д������Ļ�ѧʽ�����¼��������
�������һ�����Ԫ�ط���д���ҷ�����һԪ�ط���д�����ѱ�ʾԭ�Ӹ�����С���֣��ֱ�д��Ԫ�ط��ŵ����½ǡ���CaO��Al2O3��
�ڽ���Ԫ����ǽ���Ԫ����ɵĻ����Ӧ��д����Ԫ�ط��ţ�Ȼ����д�ǽ���Ԫ�ط��š���NaCl��KCl��
���𰸡���1��N2 ��2��Ne ��3��S ��4��Cu ��5��CaO ��6��Al2O3 ��7��NaCl ��8��KCl
��2�����й��ڻ��ϼ۵�˵���У���ȷ����
A. H2��H�Ļ��ϼ�Ϊ+1��
B. H2O����Ԫ�صĻ��ϼ�Ϊ��2��
C. һ��Ԫ��ֻ��һ�ֻ��ϼ�
D. �ǽ���Ԫ���ڸ�����Ԫ�ػ���ʱ��һ���Ը���
����������A��H2���������ʣ���Ԫ��û�и�����Ԫ�ػ��ϣ���˻��ϼ�ӦΪ��ۡ�
��B��H2O����Ԫ������Ԫ���γɵĻ������ˮ�����У�����+1�ۣ����ԣ�2�ۣ�
��B��˵����ȷ��
��C��һ��Ԫ��ֻ��һ�ֻ��ϼ۵�˵������ȷ��������ЩԪ��ֻ��һ�ֻ��ϼۣ�������Ԫ�����м��ֻ��ϼ۵ģ������Բ��ִ������塣
��D��˵������ȷ���ǽ���Ԫ���ڸ�����Ԫ�ػ���ʱ�Ը��ۣ����ǽ���Ԫ����ǽ���Ԫ�ػ���ʱ������������Ҳ�����Ը��ۡ������ڸ��⻯�����ɵ�����H2S������Ը��ۣ������ڸ�������ʱ�����ɵĶ�����������+4�ۣ�������������ʱ��+6�ۡ�
���𰸡�B
��3��X��Y����Ԫ�أ�Xԭ�ӵ��������һ�����ӣ�Ԫ��YΪ��2�ۣ���X��Y����Ԫ���γɵĻ�����Ļ�ѧʽ������
A. X2Y B. XY C.
X3Y2 D. XY2
��������XԪ��ԭ���������1�����ӣ����γɻ�����ʱ��ʧȥ1�����ӣ�ͨ���ԣ�1�ۣ���Y Ϊ��2�ۣ����ݻ������л��ϼ۴�����Ϊ0���Ƶû�ѧʽΪX2Y.
���𰸡�A
��4�����м������ʰ���Ԫ�ػ��ϼ۹�������ΪKCl�� ��HClO��KClO3��HClO4����ո��ڵ�������
A. NaCl B. NaClO C. Cl2 D. HClO3
���������������ѧʽ����Ԫ�صĻ��ϼۺ��ҳ����ϼ۵����й���
���𰸡�C
��5��1998���й�ʮ��Ƽ��ɹ�֮һ�Ǻϳ��������ء���֪�أ�Ga��ԭ�ӵĽṹʾ��ͼΪ  ����ԭ�ӵĽṹʾ��ͼΪ
����ԭ�ӵĽṹʾ��ͼΪ ![]() �����صĻ�ѧʽ�ǣ� ����
�����صĻ�ѧʽ�ǣ� ����
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
����������������û��ѧ��������ͨ�����ӽṹʾ��ͼ�������������γɻ������У����ܵ�ʧ���ӵ���Ŀ��ȷ��Ԫ�صĻ��ϼۣ�д���仯ѧʽ����ԭ���������3�����ӣ���ʧȥ�����ϼ��ԣ�3�ۣ���ԭ���������5�����ӣ��õ�3�������γ��ȶ��ṹ�����ϼ��ԣ�3�ۡ����ݻ������ﻯ�ϼ۴�����Ϊ���ԭ��ӦΪ ![]() ��
��
���𰸡�C��
��6�����Ļ��ϼ���+2�ۺ�+3�ۣ��������Ļ������У������Ǽ��ۣ�
��FeO ��Fe2O3 ��Fe��OH��3 ��FeS ��Fe3O4
�����������пɱ仯�ϼ�+2�ۺ�+3�ۣ��ڲ�ͬ�����Ļ������б��ֵĻ��ϼ۲���ͬ����Ҫ�����ڻ��������������ϼ۵Ĵ�����Ϊ���ԭ��ȥ��
���Ǹ����ۣ������ڢ�FeO�У���Ϊ+2�ۣ��ڢ�Fe2O3�У���Ϊ+3�ۡ�����������Ϊ��1�ۣ����Ԣ�Fe��OH��3�У���Ϊ+3�ۡ��������������ʱ�������ƣ���Ϊ��2�ۣ����Ԣ�FeS�У�FeΪ+2�ۡ�
��Fe3O4Ϊһ����Ļ�����������������ϼ۴�����Ϊ��ķ���ȥ�����Ļ��ϼۡ���X�����о�֤����Fe3O4��һ�ָ��ӵĻ���������ΪFe��FeO2��2����С�����ڵ���Ϊ+3�ۣ����������Ϊ+2�ۡ��ϸ�˵Fe3O4�������������ѧ��ֻ�ǰ������������Ϊ�˱�ʾ������Ļ��ϼۣ��ɰ���д��FeO��Fe2O3����ʽ��
���𰸡�![]()
![]()
��7����¼��¼��Ŵ����õĴŷۣ�����Ҫ�ɷֵĻ�ѧ���Ϊ![]() �Ļ������֪�����ܣ�Co���Ļ��ϼ�Ϊ+2�ۣ���Ԫ��ֻ��+2�ۺ�+3�ۣ���x��ֵ������Fe���Ļ��ϼ۷ֱ�Ϊ
�Ļ������֪�����ܣ�Co���Ļ��ϼ�Ϊ+2�ۣ���Ԫ��ֻ��+2�ۺ�+3�ۣ���x��ֵ������Fe���Ļ��ϼ۷ֱ�Ϊ
A. 1��+3 B.
1��+
������������Ľⷨ�����֣���һ��������֤��������ѡ���е����ִ��뵽��ѧʽ�У����û��ϼ۴�����Ϊ0���ж���������Ԫ�ػ��ϼۣ�2����3�۷ֱ����![]() ���x���ж�������. �ɵó���ȷ��ΪA. ������������۷����ɻ�ѧʽ
���x���ж�������. �ɵó���ȷ��ΪA. ������������۷����ɻ�ѧʽ![]() ����֪xֻ��Ϊ1��2���ٰ�xΪ1��2���뻯ѧʽ�������Ԫ�صĻ��ϼ�.
����֪xֻ��Ϊ1��2���ٰ�xΪ1��2���뻯ѧʽ�������Ԫ�صĻ��ϼ�.
���𰸡�A
�ġ�Ӧ������
����ʱͨ���������ָ��Ҫ���û�ѧ���ű�ʾ���ӡ����Ӹ��������ж�������Ԫ�صĻ��ϼ۵ȣ�����Ԫ�أ���ԭ���ţ��Ļ��ϼ���ȷ��д���ʵĻ�ѧʽ��ָ����ѧ���ż���Χ���ֵ����壬��ѡ��������ͬ���йط��ţ�����ͬһ���ֵIJ�ͬ���������̶ȣ�������������г������ʵ���������;��д��ѧʽ�����������ʵĻ�ѧʽ����дԭ���ж�δѧ�������ʵĻ�ѧʽ��д���Ͷ���������
Ҫ����������19�ֳ���Ԫ�صķ��ź�5��ԭ���ŵ����ƺ�д������dz���Ԫ�غ�ԭ���ŵĻ��ϼۣ������ڻ��������������ϼ۴�����Ϊ�����дԭ��Ū�廯ѧ������Χ���ֱ�ʾ�����壺�ٷ���ǰ������ֱ�ʾ���ӡ�ԭ�ӡ����ӵĸ������ڷ�����Ԫ�ط������½ǵ����ֱ�ʾ1�����ӻ�ԭ������ԭ�ӵĸ�������Ԫ�ط������Ϸ������ֱ�ʾԪ�ػ��ϼۣ���Ԫ�ط��Ż�ԭ�������Ͻǵ����ֱ�ʾ���������������
�塢����С��
1����ʶ��ѧʽ�����壨��ۡ��ۣ�
2��ԭ�ӽṹ�����ϼۡ���ѧʽ
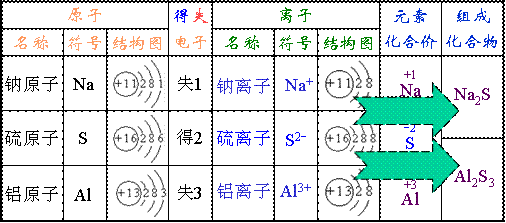
��ʶ��Ԫ�صĻ��ϼ���Ԫ�ص�ԭ�����γɻ�����ʱ���ֳ��������ʣ�������ֵ�Ǻ;��廯��������ϵ�ġ�
3�����Ӻͻ��ϼ۵�����
4����dz���Ԫ�غ�ԭ���ŵĻ��ϼۣ����ܸ��ݻ��ϼ���д��ѧʽ������ݻ�ѧʽ�жϻ��ϼۡ�
5�����ʺͻ������д��������
������ǰ˼ά���йػ�ѧʽ�ļ��㣩
1���������ʵ���Է�������=��Ԫ�ص�
��ԭ�Ӹ���֮
2�������������Ԫ�ص�������=��Ԫ��
��ԭ�Ӹ���֮
3������������ijԪ�ص���������
������ijԪ�ص���������=����Ԫ�ص����ԭ��������ԭ�Ӹ������»������ ��100%
4������һ�������Ļ������к�ijԪ�ص�����
ijԪ�ص�����=��������������������и�Ԫ�ص� ��
���Σ������������=ijԪ�ص������»������и�Ԫ�ص� ��
5����֪�������и�Ԫ�ص������Ⱥ�Ԫ�ص����ԭ����������ԭ�Ӹ�����
��Ԫ�ص�ԭ�Ӹ�����=��Ԫ�ص�����/��Ԫ�ص����ԭ������֮
��ģ�����⡿������ʱ�䣺35���ӣ�
һ��ѡ���⣺
1. �������ʵĻ�ѧʽ��д��ȷ����
A. ����пOZn B. ��������O3S
C. ����He2 D. ������CaO
2. ��֪������̼�Ļ�ѧʽΪCO2,��������˵����ȷ����
A. ��һ��̼Ԫ�غ�������Ԫ�����.
B. ��һ��̼ԭ�Ӻ�һ�������ӹ���.
C. ��̼Ԫ�غ���Ԫ������Ԫ�����.
D. һ��������̼������һ��̼ԭ�Ӻ�������ԭ�ӹ���.
3. ���з���ֻ�������������
A. ![]() B.
B. ![]() C.
C. ![]() D.
D. ![]()
4. ij���ط�������ʳ���ж���������Ϊ��ʳ��ҵ�����������ƣ�NaNO2�����¡����������е�Ԫ�صĻ��ϼ���
A. +1 B. +2 C. +3 D. +5
5. ����ɴ��������ۺ�����泥�NH4ClO4���Ļ������Ϊ����ȼ�ϣ����������Cl�Ļ��ϼ���
A. +1 B. +3 C. +5 D. +7
6. ��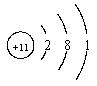 �����֡�1����ϵ���е���
�����֡�1����ϵ���е���
A. Ԫ�صĻ�ѧ���ʡ����ϼ� B. Ԫ�ص����ࡢԭ�ӵ�����
C. Ԫ�صĺ˵������ԭ�ӵ���Ŀ D. ���ʵ�״̬��ԭ�ӵ��ȶ���
7. ��ѧ�����ǹ���ͨ�õĻ�ѧ���ԣ������й�˵����ȷ����
A. 2H��ʾ2������� B. þ���ӵķ���ΪMg2+
C. O2����Ԫ�صĻ��ϼ�Ϊ��2�� D. һ����̼�Ļ�ѧʽ��Co
8. �����������У��ԡ�2���ĺ���������ȷ����
A. 2Cu�еġ�2����ʾ2��ͭԪ��
B. Fe2+�еġ�2����ʾÿ���������Ӵ���2����λ�������
C. H2S�еġ�2����ʾ1����������к���2����ԭ��
D. Al2 ![]() �л�ѧʽ�Ϸ��ġ�2����ʾ��Ԫ��Ϊ��2��
�л�ѧʽ�Ϸ��ġ�2����ʾ��Ԫ��Ϊ��2��
9. ����[KAl ��SO4��m]��������ˮ�����ڸ�������m��ֵ��
A. 1 B. 2 C. 3 D. 10
*10. H2SO3��H2SO4���������У���ͬ����
A. ���ʵ���� B. ����Ԫ������
C. ��Ԫ�ػ��ϼ� D. ��Ԫ�ػ��ϼ�
*11��Ԫ��A��Ԫ��B���γ�AB2�ͻ������A��BԪ�صĺ˵��������Ϊ
A. 13��17 B. 11��8 C. 6��8 D. 12��9
12. �������������о����е�Ԫ�أ������ǰ���Ԫ�صĻ��ϼ��ɵ͵��ߵ�˳�����еģ���NH3����N2����NO����X����N2O5�����ݹ��ɣ�X��������
A. NO2 B. NaNO2 C. N2O3 D. N2O
*13. �������ǹ���ϸ���Ļ������ʣ����ɶ��ְ����ṹ�ɵģ��Ǹ��ӵġ���Է�������������ʡ�������������������嵰�İ�����֮һ����ͼ������������ķ��ӽṹģ��ͼ�����ж��������������������ȷ����
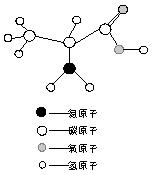
A. ����������Ļ�ѧʽΪC3H7O2N
B. ��������������У���ԭ����С
C. ���������������̼����ԭ�Ӹ�����Ϊ3��2
D. �����������ǻ����
14. �������ҵ�ʳ���Ĺ鳲;�У���һ������������Ϳ����·;�ϣ�Ϊ����������ʳ��·�����ַ�����и��ټ�������Ϣ�ص�һ�֡���������Ϣ���о������仯ѧʽΪC10H18O������Ը���Ϣ�ص�˵������ȷ����
�� ����Ϣ����C��H��O����Ԫ����ɵ�
�� ����Ϣ����C��H��O����Ԫ�ص�ԭ�Ӹ�����Ϊ10��18��1
�� ����Ϣ�أ�C10H18O������ԭ�ӹ��ɵĻ�����
�� ����Ϣ������C10H18O���ӹ��ɵ�
A. �ڡ��� B.
�١��� C.
�١��� D.
�ڡ���
15. �����������ʣ����ǰ�����˳�����Т�CO ��H2O ��NH3 ��X ��C2H4 ��P2O5 �������ǵ���ɺ����й��ɣ��ƶ�X������
A. CH3OH B. CH4 C. Fe2O3 D. SO3
��������⣺
1���Ӣ������� �������� ��������������ԭ�Ӻ˵�ѡ����ѡ����ա�
��1��ԭ�ӵĺ˵����������ԭ�ӽṹ�е�______��
��2��ԭ��������Ҫ������ԭ�ӽṹ�е�________��
��3��ԭ�ӵ����ԭ������������ԭ�ӽṹ�е�________��
��4��ԭ�ӵ�������Ҫ������ԭ�ӽṹ�е�______��
��5��Ԫ�ص����������ԭ�ӽṹ�е�______��
��6��Ԫ�صĻ�ѧ������Ҫ������ԭ�ӽṹ�е�________��
��7��ԭ�ӵ�������Ҫ������ԭ�ӽṹ�е�________ ��
��8��Ԫ�صĻ��ϼ���Ҫ������ԭ�ӽṹ�е�________��
2��д��������Ԫ�ط�����Χ�����֡�2���ֱ��ʾ�ĺ��壺
��1��O2
�� ��2��2O
��

��5��H2![]() ����6��2H2O
��
����6��2H2O
��
3��
|
Ԫ������ |
�� |
�� |
�� |
�� |
�� |
�� |
�� |
��1���ϱ�Ԫ���У��ڵؿ��ں������Ľ���Ԫ�ط����� �� �������ں�������Ԫ�ط����� ��ˮ�к��е�+1�۵�Ԫ�ط����� ��
��2���Ȼ��ƵĻ�ѧʽΪ ��Na2SO3��SԪ�صĻ��ϼ�Ϊ ��
*��3����ͼ��ʾ�������ʾ��ģ�ͣ��������ڻ�������� ������ĸ��ţ������ڻ������� ������ĸ��ţ���ѡ���ϱ���Ԫ�أ���ʾAͼ�еķ��ӣ��仯ѧʽ����Ϊ ��д�����ּ��ɣ���
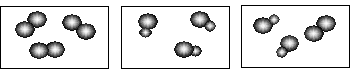
A B C
4����ѧ�Ӻ�ۺ��������Ƕ���ʶ���ʡ�
��1��ͼ��������Ԫ����Ԫ�����ڱ��е���Ϣ��ͼ������ԭ�Ӻ���ԭ�ӵ�ԭ�ӽṹʾ��ͼ��
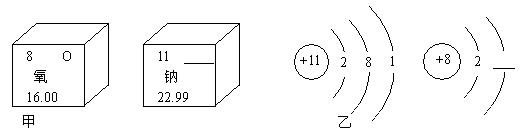
�� ͼ�ĺ���������� ��ͼ�Һ����ϵ������� ��
�� ����ͼ�ҵ���Ϣ��д�������ƵĻ�ѧʽ��������ϼ� ��
*��2���±����е��Dz���Ԫ�ص��й���Ϣ��
|
Ԫ������ |
���������� |
���ӷ��� |
�������ϼ� |
|
� |
1 |
Li+ |
+1 |
|
�� |
1 |
K+ |
+1 |
|
þ |
2 |
Mg2+ |
+2 |
|
�� |
3 |
Al3+ |
+3 |
|
�� |
6 |
O2�� |
��2 |
|
�� |
7 |
F�� |
��1 |
|
�� |
6 |
S2�� |
��2 |
���ϱ����Է���Ԫ�صĻ��ϼ�������������������������ɴ���ij�ֹ���������Ա��еĸ������ݽ��бȽϡ�������Ѱ�����еĹ��ɡ��� �� �� ��
![]()
������𰸡�
һ��ѡ���⣺
|
��� |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
�� |
D |
CD |
C |
C |
D |
A |
B |
B |
|
��� |
9 |
10 |
11 |
12 |
13 |
14 |
15 |
|
|
�� |
B |
C |
CD |
D |
D |
A |
B |
|
��������⣺
1����1������2������3���٢���4���ܣ�5������6���ۣ�7���٢���8����
2����1��һ����������������ԭ����ɣ���2��������ԭ�ӣ���3�������������ӣ���ÿ���������к�2����ԭ�ӣ���4����2�������ӣ���ÿ�������Ӵ�2����λ�ĸ���ɣ���5��ˮ����Ԫ���ԣ�2�ۣ���6��2��ˮ���ӡ�
3����1��Al O H
��2��CaCl2 +4
��3��B C H2��O2����Cl2��
4����1����Na 6 ��![]()
��2�������ϼ۵���ֵ��ԭ�ӵ������������й�
�ڻ��ϼ۵������������������һ��