![]()
б╛▒╛╜▓╜╠╙¤╨┼╧вб┐
╥╗бв╜╠╤з─┌╚▌
╡┌╢■╡е╘к╫█║╧╦╪─▄╝ь▓т
б╛─г─т╩╘╠тб┐ги┤Ё╠т╩▒╝фг║90╖╓╓╙гй
╧р╢╘╘н╫╙╓╩┴┐г║гиHбк1 Oбк16 Naбк23 Sбк
╥╗бв╤б╘ё╠тги▒╛╠т░№└и10╨б╠тгм├┐╨б╠т3╖╓гм╣▓30╖╓бг├┐╨б╠т╓╗╙╨╥╗╕І╤б╧ю╖√║╧╠т╥тгм╜л╖√║╧╠т╥т╡─╤б╧ю╨Ґ║┼╠ю╚ы╠т║ґ╡─└и║┼─┌гй
1бв
A. ║г╦о╩╟╗ь║╧╬я
B. ║г╦о╩╟▒е║═╚▄╥║
C. ║г╦о╓╨╡─╗п╤з╫╩╘┤╩о╖╓╖с╕╗ D. ║г╦о╔╣╤╬╡─╘н└э╩╟╒Є╖в╚▄╝┴╡├╡╜╛з╠х
2бв╧┬┴╨╣¤│╠╖в╔·╗п╤з▒ф╗п╡─╩╟
ги гй
в┘║г╦об░╔╣╤╬б▒ в┌║г╦об░╓╞╝юб▒ в█║г╦о╡н╗п в▄┤╙║г╦о╓╨╠с╚б├╛
A. ╚л▓┐╩╟ B. ╓╗╙╨в┌ C. ╓╗╙╨в┌в▄ D. в┘в┌в█
3бв╘┌╥╗╢и╠є╝■╧┬гм─│╬я╓╩╡─▒е║═╚▄╥║╥╗╢и╩╟
ги гй
A. ┼и╚▄╥║
B. ╝╙╚ы╕├╚▄╓╩╡─╛з╠хгм╚▄╓╩╡─╓╩┴┐╖╓╩¤▓╗╖в╔·╕─▒ф╡─╚▄╥║
C. ╜╡╬┬║ґ─▄╬І│І╛з╠х╡─╚▄╥║
D. ╒Є╖в╦о╖╓║ґ─▄╬І│І╛з╠х╡─╚▄╥║
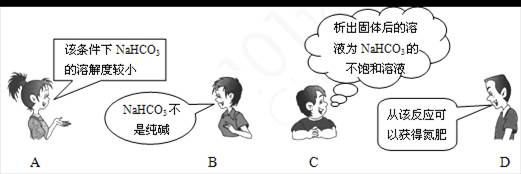
4бвб░NaCl+CO2+NH3+H2O=NaHCO3+NH4Clб▒╩╟╓Ї├√╡─б░║ю╩╧╓╞╝ю╖иб▒╡─╓╪╥к╖┤╙жбг╧┬├ц╩╟4╬╗═м╤з╢╘╕├╖┤╙ж╔ц╝░╡─╙╨╣╪╓к╩╢╖в▒э╡─▓┐╖╓╝√╜тбг╞ф╓╨▓╗╒¤╚╖╡─╩╟ ги гй
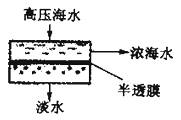
5бвс╙уЄ╩╟╕І╥╫║╡╚▒╦о╡─║г╡║╧╪. ╧╓╘┌╥└┐┐║г╦о╡н╗п╝╝╩єгм├┐╠ь┐╔╔·▓·6600╢╓╡н╦огм╜т╛І┴╦╚▒╦о╬╩╠тбг╕├╝╝╩єги╘н└э╚ч═╝╦ї╩╛гй▓╔╙├╢╘║г╦о╝╙╤╣гм║г╦о╓╨╡─╚▄╝┴╖╓╫╙┐╔╥╘═и╣¤░ы═╕─дгм╢Ї╚▄╓╩╖╓╫╙║▄─╤═╕╣¤бг╧┬┴╨╦╡╖и╒¤╚╖╡─╩╟
ги гй
A. ┼и║г╦о╓╨╚▄╓╩╓╩┴┐╘І╝╙
B. ┼и║г╦о╡─╚▄╓╩╓╩┴┐╖╓╩¤╘І┤ґ
C. ┼и║г╦о╡─╚▄╓╩╓╩┴┐╖╓╩¤╝є╨б
D. ╜т╛І┴╦╚▒╦о╬╩╠тгм╛═┐╔╥╘▓╗╙├╜┌╦о┴╦
6бв╧┬┴╨╕і╫щ╬я╓╩▓╗─▄╖в╔·╕┤╖╓╜т╖┤╙ж╡─╩╟
ги гй
A. ╧б┴Ґ╦с╙ы╟т╤є╗п─╞╚▄╥║
B. ╧б╤╬╦с╙ы┤┐╝ю╚▄╥║
C. ╧є╦с╝╪╚▄╥║╙ы┬╚╗п─╞╚▄╥║
D. ┬╚╗п═н╚▄╥║╙ы╟т╤є╗п╕╞╚▄╥║
7бв╓╗╙├╥╗╓╓╩╘╝┴└┤╝Ї▒ЁNaOHбвCaгиOHгй2бв╧б┴Ґ╦с╚¤╓╓╚▄╥║гм╒т╓╓╩╘╝┴╩╟ ги гй
A. ┬╚╗п▒╡╚▄╥║ B. ╫╧╔л╩п╚я╩╘╥║ C. ╠╝╦с─╞╚▄╥║ D. ╖╙╠к╩╘╥║
8бв╧┬═╝╩╟KNO3║═NaCl╡─╚▄╜т╢╚╟·╧▀бг╧┬┴╨╦╡╖и╓╨╒¤╚╖╡─╩╟
ги гй
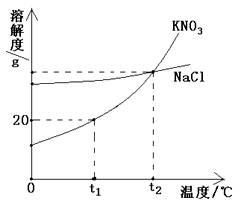
A. NaCl╡─╚▄╜т╢╚▓╗╩▄╬┬╢╚╡─╙░╧ь
B. t
C. t
D. ╘┌╬┬╢╚╕▀╙┌t
9бв╥к│¤╚е╧┬┴╨╚¤╓╓╬я╓╩╓╨╡─╔┘┴┐╘╙╓╩ги└и║┼─┌╡─╬я╓╩╬к╘╙╓╩гйгм ╝╫г║CaCO3 гиNa2CO3гй ╥╥г║NaOH гиNa2CO3гй ▒√г║KNO3гиNaClгйбг ┐╔╤б╙├╡─╩╘╝┴╝░▓┘╫і╖╜╖и╙╨г║в┘╝╙╩╩┴┐╦огм╜┴░шгм╣¤┬╦г╗ в┌╚▄╜тгм╝╙╩╩┴┐╩п╗╥╦огм╣¤┬╦гм╒Є╖вбг в█╚╚╦о╚▄╜тбк╜╡╬┬╜с╛збк╣¤┬╦
╧┬┴╨╫щ║╧╒¤╚╖╡─╩╟г║
ги гй
A. ╝╫бкв┌гм╥╥бкв█гм▒√бкв┘ B. ╝╫бкв┘гм╥╥бкв█гм▒√бкв┌
C. ╝╫бкв┌гм╥╥бкв┘гм▒√бкв█ D. ╝╫бкв┘гм╥╥бкв┌гм▒√бкв█
10бв╬к┴╦│¤╚е┤╓╤╬╓╨╗ь╙╨╡─╔┘┴┐╕╞╤╬бв├╛╤╬бв┴Ґ╦с╤╬║═─р╔│гм╡├╡╜╛л╓╞╩│╤╬╦огм┐╔╜л┤╓╤╬╚▄╙┌╦огм╚╗║ґ╜Ї╨╨╧┬┴╨▓┘╫іг║в┘╣¤┬╦гмв┌╝╙╣¤┴┐NaOH╚▄╥║гмв█╝╙╩╩┴┐╤╬╦сгмв▄╝╙╣¤┴┐Na2CO3╚▄╥║гмв▌╝╙╣¤┴┐BaCl2╚▄╥║бг╘Ґ╒¤╚╖╡─▓┘╫і╦│╨Ґ╩╟
ги гй
A. в┘в┌в█в▄в▌ B. в┌в█в▄в▌в┘
C. в▌в┌в▄в┘в█ D. в█в▌в┘в┌в▄
╢■бв╠ю┐╒╙ы╝Ґ┤Ёги▒╛╠т░№└и5╨б╠тгм╣▓43╖╓гй
11бвги4╖╓гй┤╙╥╘╧┬╬я╓╩╓╨гм╤б╘ё╩╩╡▒╡─╬я╓╩╠ю┐╒ги╠ю╨Ґ║┼гй
в┘├╠╜с║╦ в┌┤┐╝ю
в█┐╔╚╝▒ї в▄╕▀├╠╦с╝╪ в▌╩ь╩п╗╥
┐╔╙├╫і╕т╡у╡─╤╬ г╗ ▒╗┐╞╤з╝╥╙■╬кб░╬┤└┤─▄╘┤б▒╡─╚╝┴╧ г╗ ╘╠▓╪╘┌║г╡╫╡─╜Ё╩Є┐ґ╬я г╗╙├╙┌╓╨║═┴Ґ╦с│з╬█╦о╓╨╣¤┴┐╡─╦с бг
12бвги6╖╓гй╧╓╙╨╥╗╞┐╜╙╜№▒е║═╡─╟т╤є╗п╕╞╚▄╥║гм╩╘╛┘│І╚¤╓╓╩╣╞ф▒ф│╔▒е║═╚▄╥║╡─╖╜╖и
бв
бв
бг
13бвги2╖╓гй╫І┬Ї═╖╡─├ц╖█╘┌╖в╜═╩▒╗с▓·╔·╥╗╓╓╦сгм╩╣╒Є│І╡─┬Ї═╖╙╨╦с╬╢бг╚ч╣√╘┌├ц═┼╓╨╝╙╚ы╥╗╨й╠╝╦с─╞гм┐╔╩╣┬Ї═╖▓╗╦с╟╥╦╔╚эгм╞ф╘н╥Ґ╩╟ бг
14бвги13╖╓гй╤╠╠и╩╟├└└І╡─║г▒є│╟╩╨гм╙╨╜╧│д╡─║г░╢╧▀гм║г╤ґ╫╩╘┤╩о╖╓╖с╕╗бг╥╘╧┬╩╟╢╘║г╦о╫╩╘┤╡─▓┐╖╓└√╙├бг
ги1гй║г╦о╓╨║м┴┐╫ю╕▀╡─╤╬╩╟
гм║г╦о╛н
╜с╛з┐╔╗ё╡├┤╓╤╬бг
ги2гй┤╙╔╣╤╬║ґ╡─┬▒╦о╓╨┐╔╠с╚б╓╪╥к╜Ё╩Є├╛бг╠с╚б├╛╡─▓╜╓ш╚ч╧┬г║
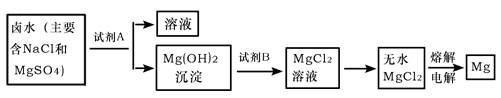
╠с╚бMg╡─╣¤│╠╓╨гм╩╘╝┴A╫ю║├╤б╙├
ги┤╙╬╥╩╨╙╨╖с╕╗╡─╩п╗╥╩п╫╩╘┤┐╝┬╟гйгм╩╘╝┴B╤б╙├
бг╥к╩╣MgSO4═ъ╚л╫к╗п╬к│┴╡эгм╝╙╚ы╩╘╝┴A╡─┴┐╙ж гм╖┤╙ж╡─╗п╤з╖╜│╠╩╜╬к
бг╡ч╜тMgCl2╡─╣¤│╠╓╨ ─▄╫к╗п╬к ─▄бг
ги3гй╧Ґ▒е║═╡─┬╚╗п─╞╚▄╥║╓╨╥└┤╬═и╚ы░▒╞Їбв╢■╤є╗п╠╝гм╬І│І╠╝╦с╟т─╞╛з╠хгм╝╙╚╚╠╝╦с╟т─╞╛з╠х┐╔╓╞╡├┤┐╝юбг╨┤│І╔╧╩І╖┤╙ж╡─╗п╤з╖╜│╠╩╜г║
в┘
г╗
в┌
бг
15бвги5╖╓гй╝Ї▒Ё╤╬╦сбв╟т╤є╗п─╞бв╠╝╦с─╞║═┬╚╗п─╞╦─╓╓╬▐╔л╚▄╥║бг╕і╚б╔┘┴┐гм╖╓▒Ё╝╙╚ы╦─╓з╩╘╣▄╓╨гм╘┘╖╓▒Ё╧Ґ╒т╦─╓з╩╘╣▄╓╨╡╬╚ы╫╧╔л╩п╚я╩╘╥║бг╧╚▒╗╝Ї▒Ё│І└┤╡─┴╜╓╓╬я╓╩╖╓▒Ё╬к бв г╗╝Ї▒Ё┴э═т┴╜╓╓╚▄╥║─у╤б╙├╡─╩╘╝┴╩╟ ги╠ю╗п╤з╩╜гйгм╙╨╣╪╡─╖╜│╠╩╜╬к
бг
16бвги7╖╓гй╝╫бв╥╥бв▒√╚¤╓╓╬я╓╩╡─╚▄╜т╢╚╟·╧▀╚ч═╝╦ї╩╛гм╛▌═╝╗╪┤Ёг║
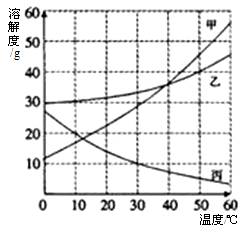
ги1гй
ги2гй
ги3гй╥к╩╣▒е║═╡─▒√╚▄╥║▒ф╬к▓╗▒е║═╚▄╥║гм┐╔▓╔╚б╡─┤ы╩й╩╟
бв
г╗
ги4гй
ги5гй
ги6гй╚Є╝╫╓╨║м╔┘┴┐╥╥гм╙ж╙├
╡─╖╜╖и╠с┤┐╝╫бг
17бвги6╖╓гй╬к┴╦│¤╚е┬╚╗п─╞╤ї╞╖╓╨╡─╠╝╦с─╞╘╙╓╩гм╨╦╚д╨б╫щ╫ю│є╔ш╝╞┴╦╚ч╧┬╡─╖╜░╕▓в╜Ї╨╨╩╘╤щбг
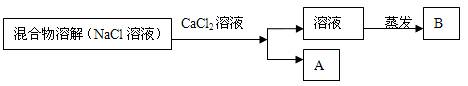
ги1гй╨┤│І│┴╡эA╡─╗п╤з╩╜
бг
ги2гй╝╙╚ыCaCl2╚▄╥║║ґгм╖╓└ы│¤╚е│┴╡эA╡─╩╡╤щ▓┘╫і╖╜╖и╩╟ бг
ги3гй═м╤з╘┌╩╡╤щ╣¤│╠╓╨гм╙╓╖в╧╓┴╦╨┬╡─╬╩╠тг║┤╦╖╜░╕║▄╚▌╥╫╥¤╚ы╨┬╡─╘╙╓╩гм╟ы╨┤│І╣╠╠х╬я╓╩B╡─│╔╖╓
ги╙├╗п╤з╩╜▒э╩╛гйбг
ги4гй═м╤з╝╠╨Ї╠╜╛┐║ґ╙╓╠с│І╨┬╡─╖╜░╕г║╜л╗ь║╧╬я╚▄╜тгм╡╬╝╙╤╬╦с╓┴▓╗╘┘▓·╔·╞Ї╠х╬к╓╣гм╘Ґ╝╚─▄│¤╚е╠╝╦с─╞╘╙╓╩гм╙╓─▄╙╨╨з╡─╖└╓╣╨┬╘╙╓╩╡─╥¤╚ыбг╨┤│І╙╨╣╪╖┤╙ж╡─╗п╤з╖╜│╠╩╜г║
бг
╚¤бв╩╡╤щ╠╜╛┐╠тги▒╛╠т░№└и2╕І╨б╠тгм╣▓17╖╓гй
18бвги11╖╓гй╩╡╤щ╓╨╤з═м╤з┐к╒╣╕┤╖╓╜т╖┤╙ж╤╨╛┐╨╘╤з╧░гм╔ш╝╞┴╦╚ч╧┬╤╨╛┐╨╘╤з╧░╦╝┬╖г║
б╛┴╖╧░╓╩╥╔б┐╧┬┴╨╕і╫щ╬я╓╩╝ф╛ї─▄╖┤╙жгм╨┤│Ів█бвв▄╖┤╙ж╡─╗п╤з╖╜│╠╩╜бг
в┘╟т╤є╗п─╞╚▄╥║╙ы╤╬╦с в┌╠╝╦с─╞╚▄╥║╙ы┴Ґ╦с
в█┴Ґ╦с═н╚▄╥║║═╟т╤є╗п─╞╚▄╥║
бг
в▄╠╝╦с─╞╚▄╥║║═┬╚╗п▒╡╚▄╥║
бг
б╛╤╨╛┐╠╓┬█б┐╔╧╩І╖┤╙ж╬к╩▓├┤─▄╣╗╖в╔·г┐╩╟╥Ґ╬к╒т╨й╖┤╙ж╬я╓╨║м╙╨╠╪╩т╡─╥єбв╤Є└ы╫╙гм╚чв┘╓╨╙╨H+║═OHгнгмв┌╓╨╙╨H+║═CO32гнгмв█╓╨╙╨
гмв▄╓╨╙╨
бг
б╛╣╣╜и═Ї┬чб┐░┤╒╒╥╗╢и╡─╦│╨Ґ┼┼┴╨╒т╨й└ы╫╙гм╛═┐╔╥╘╨╬│╔╥╗╓╓═Ї┬ч╨╬╩╜бг╘┌═Ї┬ч╓╨гм╙├╢╠╧▀╧р┴м╡─╒т╨й╥єбв╤Є└ы╫╙─▄┴╜┴╜╜с║╧╔·│╔│┴╡э╗Ґ╞Ї╠х╗Ґ╦обг╧╓╙╨Ca2+бвSO42гнгм╟ы╜л╦№├╟╠ю╚ы╧┬├ц║╧╩╩╡─б░ги гйб▒╓╨гм╩╣╞ф╨╬│╔╥╗╕І╕№╬к═ъ╒√╡─╕┤╖╓╜т╖┤╙ж═Ї┬чбг
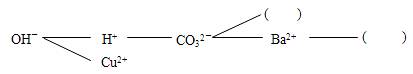
б╛═╪╒╣╘╦╙├б┐═и╣¤╨╬│╔╡─═Ї┬чгм┐╔╥╘┼╨╢╧╗п║╧╬я╝ф─▄╖ё╣▓┤цгм╜Ї╨╨╬я╓╩╡─╝Ї▒Ёгм╙├╙┌╬я╓╩╡─│¤╘╙╡╚бг╚ч╟т╤є╗п─╞╚▄╥║╗ь╙╨╠╝╦с─╞гм┐╔╥╘╝╙╚ы
ги╠ю╨┤╗п╤з╩╜гй│¤╚е╠╝╦с─╞бг
19бвги6╖╓гй╣д╥╡╔╧│г╙├╡ч╜т┤┐╛╗╡─▒е║═╩│╤╬╦о└┤╓╞╔╒╝юбг╜л╓╞╡├╡─╔╒╝ю╚▄╥║╘┘╛н┼и╦єбв╒Є╖в╡╚▓╜╓ш╓╞│╔╣╠╠х╔╒╝юбг╬╥├╟╓к╡└гм╘н┴╧═ї═ї▓╗─▄╚л▓┐╫к╗п╬к╔╒╝югиNaOHгйг╗┴э═тгм╚ч╣√╣╠╠х╔╒╝ю│д╩▒╝ф╘┌▓╓┐т╖┼╓├гм▒э├ц┐╔─▄╗с╙╨Na2CO3╘╙╓╩╔·│╔бг
ги1гй╧╓┤╙▓╓┐т╓╨╚б└┤╔╒╝ю╤ї╞╖гм╟ы─у═╞╢╧гм╕├╔╒╝ю╤ї╞╖╓╨┐╔─▄║мNa2CO3╘╙╓╩═тгм╗╣┐╔─▄║м╙╨╡─┴э╥╗╓╓╘╙╓╩╩╟
бг
ги2гй╥к╝ь╤щ╤ї╞╖╓╨┐╔─▄║м╙╨╡─╒т┴╜╓╓╘╙╓╩гм╟ы─у═ъ│╔╧┬┴╨╡─╩╡╤щ╔ш╝╞╖╜░╕бг
|
╩╡╤щ▓╜╓ш |
╩╡╤щ╧╓╧ґ |
╜с┬█ |
|
1бв╚б╔┘┴┐╤ї╞╖╙┌╩╘╣▄╓╨▓в╝╙╚ы╣¤┴┐╡─╧бHNO3 |
|
|
|
2бв╘┘╧Ґ╩╡╤щв┘╡─╚▄╥║╓╨╝╙╚ыAgNO3╚▄╥║ |
|
|
╦─бв╝╞╦у╠тги▒╛╠т░№└и1╕І╨б╠тгм╣▓10╖╓гй
20бв╧Ґ
╟ґг║в┘▓·╔·╢■╤є╗п╠╝╡─╓╩┴┐бг
в┌╖┤╙ж║ґ╦ї╡├╚▄╥║╡─╓╩┴┐╖╓╩¤бг
│м╟░╦╝╬мг║
╡┌╥╗╡е╘кб╢│г╝√╡─╦с║═╝юб╖
1бв╦с╝ю╓╕╩╛╝┴бв╦с╝ю╩╘╓╜бвpH╩╘╓╜бв╚▄╥║╡─╦с╝ю╨╘бв╦с╝ю╢╚
2бв╦сбв╝юбв╤╬╡─╢и╥хбв╫щ│╔бв╖╓└рбв├№├√╝░┼╨╢╧
3бв╝╕╓╓│г╝√╡─╦с║═╝ю╡─╦╫├√бв╬я└э╨╘╓╩бв╠╪╨╘бв╩╣╙├╖╜╖и╝░╙├═╛
4бв╦сбв╝ю╡─╗п╤з╨╘╓╩гм╙╨╣╪╗п╤з╖╜│╠╩╜╡─╩щ╨┤бв╧╓╧ґ╝░╙╨╣╪╡─╩╡╤щ╠╜╛┐
5бв╓╨║═╖┤╙жбв╕┤╖╓╜т╖┤╙ж
╡┌╢■╡е╘кб╢║г╦о╓╨╡─╗п╤зб╖
1бв║г╦о╓╨╡─╬я╓╩бв║г╡╫┐ґ╬ябв║г╤ґ╫╩╘┤┐к╖вбв└√╙├╝░▒г╗д
2бв║г╦о╠с├╛бв║г╦о╡н╗пбв║г╦об░╔╣╤╬б▒бв║г╦об░╓╞╝юб▒
3бв▒е║═╚▄╥║бв▓╗▒е║═╚▄╥║бв╜с╛збв╚▄╜т╢╚бв╚▄╜т╢╚╟·╧▀
4бв┤╓╤╬╡─╠с┤┐ги▓╗╚▄╨╘╘╙╓╩бв┐╔╚▄╨╘╘╙╓╩гй
5бв┤┐╝ю╡╚╤╬└р╬я╓╩╡─╓╪╥к╨╘╓╩
![]()
б╛╩╘╠т┤Ё░╕б┐
╥╗бв╤б╘ё╠тг║ги▒╛╠т░№└и10╨б╠тгм├┐╨б╠т3╖╓гм╣▓30╖╓гй
|
╠т║┼ |
1 |
2 |
3 |
4 |
5 |
|
┤Ё░╕ |
B |
C |
B |
C |
B |
|
╠т║┼ |
6 |
7 |
8 |
9 |
10 |
|
┤Ё░╕ |
C |
C |
D |
D |
C |
╢■бв╠ю┐╒╙ы╝Ґ┤Ё
11бвв┌ в█ в┘ в▌
12бв╘І╝╙╚▄╓╩бв╒Є╖в╦о╖╓бв╔¤╕▀╬┬╢╚
13бв╠╝╦с─╞─▄╣╗║═╖в╜═╩▒▓·╔·╡─╦с╖в╔·╖┤╙жгм╔·│╔╢■╤є╗п╠╝╞Ї╠хгм╩╣┬Ї═╖╨╬│╔║▄╢р╨б┐╫гм▒ф╡├╦╔╚э
14бвги1гй┬╚╗п─╞ ╒Є╖в
ги2гй╩п╗╥╚щ ╤╬╦с ╣¤┴┐ MgSO4+CaгиOHгй2==MgгиOHгй2б¤+ CaSO4 ╡ч ╗п╤з
ги3гйв┘NaCl+NH3+
CO2+H2O=NaHCO3+NH4Cl
в┌2NaHCO3![]() Na2CO3+H2O+CO2б№
Na2CO3+H2O+CO2б№
15бв╤╬╦с ┬╚╗п─╞ CaгиOHгй2 CaгиOHгй2+Na2CO3=CaCO3б¤+
2NaOHги║╧└э╝┤┐╔гй
16бвги1гй40 ги2гй ╥╥бв╝╫бв▒√
ги3гй╜╡╡═╬┬╢╚бв╘І╝╙╚▄╝┴ги╦огй╡─┴┐ ги4гй─▄ ги5гй╝╫ги6гй╜╡╬┬╜с╛зги╝┤└ф╚┤╚╚▒е║═╚▄╥║╖игй
17бвги1гйCaCO3 ги2гй╣¤┬╦ ги3гй NaCl║═CaCl2 ги4гйNa2CO3+2HCl=2NaCl+
H2O+ CO2б№
╚¤бв╩╡╤щ╠╜╛┐╠т
18бвб╛┴╖╧░╓╩╥╔б┐в█CuSO4 + 2NaOH = CuгиOHгй2б¤+Na2SO4
в▄ BaCl2+Na2CO3=BaCO3б¤+
2NaCl
б╛╤╨╛┐╠╓┬█б┐в█Cu2+ ║═ OHгн
в▄Ba2+ ║═CO32-
б╛╣╣╜и═Ї┬чб┐Ca2+ SO42-
б╛═╪╒╣╘╦╙├б┐CaгиOHгй2╗ҐBaгиOHгй2
19бвги1гй┬╚╗п─╞
ги2гй
|
|
|
|
|
|
╙╨╞Ї┼▌▓·╔· |
║м╙╨Na2CO3 |
|
|
╙╨░╫╔л│┴╡э╔·│╔ |
║м╙╨NaCl |
╦─бв╝╞╦у╠т
20бв╜тг║╔ш▓·╔·╢■╤є╗п╠╝╡─╓╩┴┐╬кxгм╔·│╔Na2SO4╡─╓╩┴┐╬кy
Na2CO3глH2SO4г╜Na2SO4глH2OглCO2б№
106
142
44
106г║142=
106г║44=
╖┤╙ж║ґ╦ї╡├╚▄╥║╡─╓╩┴┐╖╓╩¤╩╟г║
┤Ёг║▓·╔·╢■╤є╗п╠╝╡─╓╩┴┐╬к