![]()
【本讲教育信息】
一. 教学内容
生活中的酸和碱
二、学习目标
1. 学会用酸碱指示剂、酸碱试纸检验溶液酸碱性,知道pH与溶液酸碱性强弱的关系,会用pH试纸检验溶液酸碱性强弱。
2. 从电离的角度了解酸和碱两类化合物溶于水时发生变化的特征,理解酸和碱的定义。
3. 从H+ 、OH-的角度认识溶液呈酸碱性的原因,进一步建立宏观与微观相联系的思维方式。
4. 通过实验探究,初步学会运用间接观察的方法收集证据。
5. 了解溶液的酸碱性对生命活动的重要意义,增强对化学学习的情感。
三、全面突破
知识点(一):如何识别酸和碱

3、酸和碱
①定义:电离时生成的阳离子全部是氢离子(H+)的化合物叫做酸.
电离时生成的阴离子全部是氢氧根离子(OH-)的化合物叫做碱.
②特征:酸电离时产生的唯一的阳离子是氢离子
碱电离时产生的唯一的阴离子是氢氧根离子
③酸和碱的判断
从组成看:酸→H+ + 酸根离子; 碱→金属阳离子+ OH- 。
从名称看:酸可分为含氧酸和无氧酸,含氧酸常读作“某酸”,如碳酸(H2CO3)等;无氧酸常读作“氢某酸”,如氢氯酸(HCl)等
4、原子团:在许多化学反应里,作为一个整体参加反应,好像一个原子一样,这样的原子集团叫做原子团。原子团不能独立存在,它们在溶液中以离子的形式存在。常见的原子团有:氢氧根(![]() )、碳酸根(
)、碳酸根(![]() )、硫酸根(
)、硫酸根(![]() )、硝酸根(
)、硝酸根(![]() )、铵根(
)、铵根(![]() )。
)。
它们常作为一个整体参加化学反应
【典型例题】
例1. 下列说法中不正确的是( )。
A、石蕊试液是一种酸碱指示剂; B、酸溶液能使红色石蕊试纸变蓝;
C、酸溶液中都含有氢离子;
D、碱溶液中都含有氢氧根离子;
解析:红色石蕊试纸遇碱溶液变蓝色,用来检验碱性溶液;蓝色石蕊试纸遇酸溶液变红色,用来检验酸性溶液。
答案:B
例2. 向某无色溶液中滴入无色酚酞试液后不变色,向该溶液中滴入紫色石蕊试液则( )
A、一定显红色 B、可能仍为紫色,也可能显红色
C、一定显无色 D、可能显蓝色
解析:无色酚酞试液遇到酸性溶液和中性溶液均不改变颜色,故滴入无色酚酞试液后不变色的溶液,可能呈酸性,也可能呈中性。
答案:B
例3. 有关酸碱的叙述中正确的是( )
A、能电离产生氢离子的化合物是酸,能电离产生氢氧根离子的化合物是碱
B、溶于水使水溶液呈酸性的物质是酸,溶于水使水溶液呈碱性的物质是碱
C、酸和碱在组成上都必须含有氢元素
D、酸和碱可使石蕊试液变色,酸都可使紫色石蕊试液变红色,碱都可使石蕊试液变蓝色
解析;(1)电离时生成的阳离子全部是氢离子(H+)的化合物叫做酸.电离时生成的阴离子全部是氢氧根离子(OH-)的化合物叫做碱.
(2)酸溶液一定显酸性,但显酸性的溶液不一定是酸的溶液,也可以是一些盐的溶液;碱溶液一定显碱性,但显碱性的溶液不一定是碱的溶液,也可以是一些盐的溶液。
(3)酸或碱对酸碱指示剂的作用,实际上是H+、OH-对指示剂的作用,因此,难溶性的酸或碱对指示剂无改变颜色的作用。
答案:C
例4. 某中学化学兴趣小组的同学,用自制的酸碱指示剂对硝酸钾、氢氧化钠、盐酸等溶液的酸碱性进行测定,结果记录如下:
|
植物的汁液 |
在盐酸中 |
在硝酸钾中 |
在氢氧化钠中 |
|
牵牛花瓣 |
红色 |
紫色 |
蓝色 |
|
胡萝卜 |
橙色 |
橙色 |
橙色 |
|
月季花瓣 |
浅红色 |
红色 |
黄色 |
(1)经过探究,发现
根本不宜作酸碱指示剂,这三种物质中理想的指示剂是 。
(2)小明是一个勤于思考、喜欢钻研的同学,发现了牵牛花瓣汁液遇氢氧化钠溶液变成蓝色后,思考到了一个问题:氢氧化钠溶液中到底是哪种粒子使牵牛花瓣汁液显蓝色的呢?于是他和同学们继续探究:
【提出问题】氢氧化钠溶液中何种粒子使牵牛花瓣汁液发生颜色改变?
【查找资料】NaOH溶液中存在的粒子有大量的H2O、 Na+ 、OH― 和极少量的H+ 。
【提出猜想】猜想1:使牵牛花瓣汁液变色的粒子是H2O。
猜想2:使牵牛花瓣汁液变色的粒子是 。
猜想3:使牵牛花瓣汁液变色的粒子是 。
【设计实验】①在一支干净试管中加入2mL蒸馏水,再滴入几滴牵牛花瓣汁液,溶液几乎不变色,说明
;
②在一支干净试管中加入2mL氯化钠溶液,再滴入几滴牵牛花瓣汁液,溶液几乎不变色,说明____________________________________;
③________________________________________________。
【获得结论】原猜想
成立。(填序号)
【交流与反思】实验完毕后,继续讨论发现,还有更简单的方法,请你用文字或图示设计出更简单的方案。__________________________________________________________。
解析:(1)在酸碱盐溶液中,胡萝卜汁液颜色不发生变化,因此不宜作酸碱指示剂;牵牛花瓣汁液颜色变化最为明显,因此是理想的指示剂。
(2)实验方法:分别向只含有一种被测粒子的溶液中滴入牵牛花瓣汁液,观察颜色是否变化,即可判断是何种粒子使牵牛花瓣汁液发生颜色改变。
答案:(1)胡萝卜汁液
牵牛花瓣汁液
(2)【提出猜想】Na+ OH-
【设计实验】①使牵牛花瓣汁液变色的粒子不是H2O分子;②使牵牛花瓣汁液变色的粒子不是Na+;③在一支干净试管中加入2mL氢氧化钠溶液,再滴入几滴牵牛花瓣汁液,溶液变为蓝色,说明使牵牛花瓣汁液变色的粒子是OH-。
【获得结论】3
【交流与反思】用Ca(OH)2溶液和NaOH溶液做对照实验,运用控制变量法的思想来确定使牵牛花瓣汁液变色的粒子是OH―。
知识点(二)溶液酸碱性的强弱程度
酸溶液中都含有H+,使溶液呈酸性;溶液显酸性,说明溶液中有 H+ ,但并不是只有酸的溶液中才有H+。碱溶液中都含有OH-,使溶液显碱性;溶液显碱性,说明溶液中有OH-,但并不是只有碱的溶液中才有OH-。
在一定量的水溶液中,H+的数量越多酸性越强,OH-的数量越多碱性越强。溶液的酸碱性强弱程度,即溶液的酸碱度,通常用pH来表示。
1、pH:用来表示溶液的酸碱度
2、取值范围:0―14(pH的数值可以超出0―14,这里是说在一般情况下,溶液的pH在0―14范围内)
3、溶液的酸碱性与溶液的pH的关系:
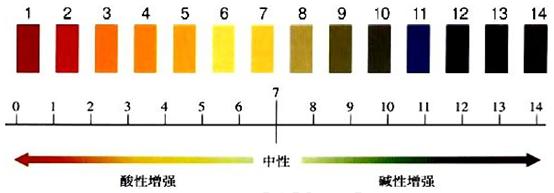
4、pH的测定方法:
①pH试纸:粗略测定,所测数值为整数。
注意:不能将pH试纸直接浸入待测溶液中测定;不能将pH试纸用水润湿后再使用。
②pH计:较精确测定,可以测量出小数。

5、改变溶液的pH的方法
①加水
②加酸碱性相同,pH不同的溶液
③加入酸碱性相反的溶液
【典型例题】
例5. 小明同学在实验室中测定某未知溶液的pH,他的实验操作如下:先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取待测试液于pH试纸上进行测定,你认为小明同学这样测得的结果与该溶液的实际pH比较将
( )
A.
偏低
B. 偏高
C. 不变
D. 无法确定
解析:先用蒸馏水将pH试纸润湿,然后用玻璃棒蘸取待测试液滴于pH试纸上,事实上已经对待测溶液进行了稀释,溶液的酸碱度可能会发生变化,但由于原待测溶液的酸碱性是怎样的还不能确定,故该待测液的pH 也就无法确定。
答案:D
例6. 甲乙两同学想了解碳酸钾溶液的酸碱性。他们分别做了以下研究:

【猜想与假设】碳酸钾溶液的酸碱性可能有 种情况。
【设计实验】用pH试纸来检测碳酸钾溶液的酸碱性。
【结论与分析】根据两位同学的实验可得出碳酸钾溶液酸碱性的结论是
。
【评价与反思】根据两位同学的实验操作,你认为
同学操作不规范。为什么?
。
如果实验室没有pH试纸,又要一次测定未知溶液的酸碱性,可选用 试液来进行实验。
解析:该题为溶液酸碱性的探究题目,任何一种溶液的酸碱性都有三种情况,即呈酸性、中性或碱性。pH试纸可以检测溶液的酸碱度,自然也就确定了溶液的酸碱性。pH试纸的正确使用方法是:用玻璃棒蘸取待测溶液滴在pH试纸上,将显示的颜色与标准比色卡对照。
答案:三 碳酸钾溶液显碱性 乙 乙同学将pH试纸直接浸入待测溶液中了 石蕊
知识点(三)酸和碱对生命活动的意义
1、测定人体内或排出的液体的pH可以了解人体的健康状况。
①健康人体的血浆的pH值在7.35 到7.45 之间,属于碱性体质者;多达70%的人是酸性体质,体液的pH值经常徘徊在7.35左右或稍低,身体处于健康和疾病之间的亚健康状态。
②人体内pH最小的分泌物是胃液(主要成分是盐酸),通常pH在0.8―1.5之间。
③人剧烈运动时,血浆的pH会变小原因:运动后肌肉酸痛是因为产生了乳酸。
2、生活中:大多数的水果为酸性;厨房中食醋为酸性,食盐为中性,碱面为碱性,厨房用的洗洁精为碱性;卫生间用的洁厕净为酸性,洗衣粉、肥皂等为碱性。
3、测定雨水的pH可以了解空气的污染情况(正常雨水的pH约为5.6,酸雨的pH小于5.6)。

4、在农业生产中,农作物一般适宜在接近中性的土壤中生长,若pH小于4或大于8,作物就不能正常生长。
5、化工生产中许多反应必须在一定的pH溶液中才能发生。
【典型例题】
例7. 人体内的一些液体的正常pH范围如下表,正常情况下,这些液体中一定呈酸性的是( )
|
|
血浆 |
乳汁 |
唾液 |
胆汁 |
胰液 |
胃液 |
|
pH范围 |
7.35~7.45 |
6.6~7.6 |
6.6~7.1 |
7.1~7.3 |
7.5~8.0 |
0.9~1.5 |
A. 胃液 B. 血浆 C. 乳汁 D. 唾液
解析:pH<7,溶液为酸性,pH越小,酸性越强;pH=7,溶液为中性;pH>7,溶液为碱性,pH越大,碱性越强。
答案:A
例8. 小明同学想利用自己所学的知识,帮助校园绿化工人做花圃土壤分析,他首先查阅资料得知了几种植物适合生长的pH范围(如下表所示)然后他取了花圃土壤样品进行检测
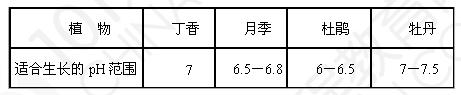
1. 请试着写出他的检测方法(
)
2. 检测结果发现土壤pH小于7,你认为花圃适宜种植哪些植物?( )
A.丁香 B.月季 C.杜鹃
D.牡丹
解析:通过查阅资料,然后进行实验,属于科学探究中的实验法。大多数植物适宜在pH接近中性的土壤中生长,由于该土壤的pH小于7,而牡丹适合生长的pH范围为7-7.5,故该花圃适宜种植的植物是月季和杜鹃。
答案:实验法 BC
四、考场清单
本讲知识,主要以选择题、填空题、探究题的形式进行出题,通常结合生产生活实际考查学生学以致用的情况。
考点1、酸碱指示剂、酸碱试纸
考点2、酸和碱的定义、组成、判断
考点3、pH与溶液酸碱性强弱的关系,pH的测定方法。
考点4、溶液的酸碱性对生命活动的重要意义
考点5、原子团
五、本讲小结
知识结构:
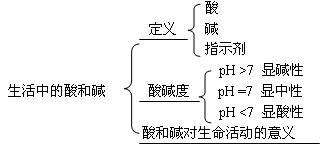
![]()
规律方法:
1、酸碱指示剂只能用来测定溶液的酸碱性;pH试纸不但可以测定溶液的酸碱性强弱,也可以测定溶液的酸碱性。
2、鉴别酸性、碱性、中性溶液时,一般用石蕊试液而不用酚酞。因为酚酞试液本身无色,酸性或中性溶液对酚酞试液都没有改变颜色的作用,用酚酞试液不能把酸性溶液和中性溶液鉴别开来。
疑难辨析:
1、和酸碱指示剂反应,变色的是指示剂,而不是酸、碱溶液。
2、酸溶液一定显酸性,但显酸性的溶液不一定是酸的溶液,也可以是一些盐的溶液;
碱溶液一定显碱性,但显碱性的溶液不一定是碱的溶液,也可以是一些盐的溶液。
3、酸或碱对酸碱指示剂的作用,实际上是H+、OH-对指示剂的作用,因此,难溶性的酸或碱对指示剂无改变颜色的作用。
六、超前思维(中和反应)
1、 与 作用生成 的反应,叫做中和反应。表示式是
。
2、中和反应的实质是 。
3、由 和 组成的化合物,叫做盐。例如 、 等。
4、写出:盐酸和氢氧化钠反应的化学方程式 ;
盐酸与氢氧化钙反应的化学方程式 。
5、人的胃中含有胃酸(HCl),如果胃酸过多,就闹胃病。此时医生常让病人服用含 的药物,帮助他们中和掉过多的胃酸来治疗。
6、改良酸性土壤常向土壤中撒 或
。
【模拟试题】(答题时间:35分钟)
一、选择题
1、生活中常见的柠檬汁、番茄汁、酸奶等物质的水溶液都有一定的酸性,这是由于它们( )
A、溶于水时都生成了盐酸 B、溶液中含有酸分子
C、组成中都含有氢元素
D、溶于水时都能电离出氢离子
2、某同学从资料上获悉,一些紫色的叶或花瓣的浸出液具有类似于石蕊试液的性质。如果他想知道紫色喇叭花是否具有这种性质,应把花瓣浸出液分别滴入下列哪组物质中进行观察( )
A、食醋、碱性肥皂水 B、食醋、酸奶
C、糖水、酸奶 D、食醋、食盐水
3、含有下列各组离子的溶液,其中的溶质都属于酸的是( )
A、Na+、H+、SO42- B、Ca2+、OH-、NO3-
C、H+、SO42-、Cl-
D、K+、CO32-、NO3-
4、能一次性区别柠檬汁、食盐水、石灰水三种溶液的是( )
A、无色酚酞试液 B、紫色石蕊试液
C、蓝色石蕊试纸 D、红色石蕊试纸
5、两种溶液混合后未发生化学反应,测得混合后溶液的pH等于5,则这两种溶液的pH可能是( )
A、1和4 B、5和7 C、3和6 D、7和9
6、下面是农作物生长时对土壤pH要求的范围,某地区经常降酸雨,以下农作物最不适宜种植的是 ( )
|
|
A |
B |
C |
D |
|
农作物 |
茶 |
西瓜 |
大豆 |
甜菜 |
|
pH范围 |
5~5.5 |
6 |
6~7 |
7~7.5 |
(双选)7、下列说法正确的是( )
A、pH为2的盐酸溶液比pH为3的盐酸溶液酸性强
B、pH 为10的氢氧化钠溶液比pH 为12的氢氧化钠溶液碱性强
C、氢氧化钠溶液能使红色石蕊试纸变蓝
D、pH的大小可表示溶液酸碱性的相对强弱程度,但它的数值不会为零
*8、在生活生产和科学实验中常用pH试纸测定溶液的pH。以下测定操作正确的是( )
A、将被测溶液滴到放在玻璃片上的pH试纸上,显色后,与标准比色卡比较
B、将pH试纸直接投入被测液中,显色后,取出与标准比色卡比较
C、先用少量水湿润试纸,后滴入被测液,显色后,与标准比色卡比较
D、先用蒸馏水清洗滴管,随后吸取被测液滴到试纸上,显色后,与标准比色卡比较
9、晓佳同学为了测定肥皂水的pH,先把pH试纸用水润湿,然后将肥皂水用玻璃棒滴到试纸上,她所测得的值与真实值相比( )
A、偏大 B、偏小 C、不变 D、以上都有可能
10、营养学上依据食品在人体中代谢产物的酸碱性,一般将食品分成酸性食品和碱性食品。其中显碱性的酸性食品是( )
|
|
A |
B |
C |
D |
|
食品 |
鸡蛋清 |
葡萄 |
苹果 |
草莓 |
|
食品类型 |
酸性食品 |
碱性食品 |
碱性食品 |
酸性食品 |
|
pH |
7.6~8.0 |
3.5~4.5 |
2.9~3.3 |
3.0~3.5 |
二、填空题
11、化学上常用酸碱指示剂测得溶液的
,常用pH试纸测得溶液的
。
12、新鲜牛奶的pH值约为7,接近____性。储存了一段时间后味道变酸,pH____。
*13、(1)用pH试纸测定溶液的pH时,正确的操作是
。
(2)小丽用pH试纸测得洗发剂的pH略大于7,则洗发剂显 性;测得护发剂的pH略小于7,则护发剂显
性。
(3)洗涤剂呈弱酸性有益于头发的健康。想一想,洗发时应先用 剂,后用 剂。
14、“果导片”是一种常用缓泻剂,主要成分是酚酞。某同学欲将其作为酚酞指示剂的替代品,他将“果导片”研成粉末放入酒精中,搅拌、静置,取上层清液滴入白醋和食盐水,看到溶液
,滴入澄清石灰水发现溶液
,确定“果导片”可作为酸碱指示剂使用。当他用饮料吸管向滴有“果导片”清液的澄清石灰水吹气时,可观察到___________________现象。
三、实验探究题
*15、南南同学跟妈妈学烧紫甘蓝(紫卷心菜),用油炒后加入食醋,发现紫色的叶片立即变红,激发了他的探究欲望。
【提出问题】紫甘蓝的汁液能做酸碱指示剂吗?
【进行实验】取紫甘蓝叶片少许在研钵中捣烂,用少量水浸泡,滤出蓝紫色的汁液。将汁液分别滴入下列液体中,观察其显示的颜色并记录。
|
液体名称 |
白醋 |
蒸馏水 |
食盐溶液 |
肥皂水 |
纯碱溶液 |
|
紫甘蓝汁液 显示的颜色 |
红色 |
蓝紫色 |
蓝紫色 |
蓝色 |
绿色 |
【得出结论1】紫甘蓝的汁液 (填“能”或“不能”)作酸碱指示剂。
【质疑并求证】紫甘蓝的汁液在均为碱性的肥皂水和纯碱溶液中,为何显示不同颜色?
用pH试纸测得上述肥皂水和纯碱溶液的pH分别为9和11,则肥皂水的碱性比纯碱溶液的碱性 (填“强”或“弱”)。
查阅资料:

【得出结论2】紫甘蓝汁液在不同pH范围内显示的颜色不同,利用紫甘蓝的汁液还可以区分液体碱性的 。
【拓展应用】柠檬酸是制汽水的原料之一,为探究其固体是否显酸性,南南同学联想到教材上二氧化碳相关实验的设计,准备了三朵用紫甘蓝的汁液染成蓝紫色的干燥小花。
取干燥的花①和喷上水的花②,分别放入盛满二氧化碳的两个集气瓶中,发现花①不变色,花②变成了 色。在干燥的花③上直接撒少量柠檬酸固体,花不变色,说明了_________________;再向该花喷水,蓝紫色的花上出现了红色。
【反思】上述花的变色均与水有关,水的作用分别是:花②中 ;花③中
。
![]()
【试题答案】
一、选择题:
|
题号 |
1 |
2 |
3 |
4 |
5 |
|
答案 |
D |
A |
C |
B |
C |
|
题号 |
6 |
7 |
8 |
9 |
10 |
|
答案 |
D |
AC |
A |
B |
A |
二、填空题
11、酸碱性 酸碱度
12、中 小于7
13、(1)用玻璃棒蘸待测溶液滴在pH试纸上,将显示的颜色与标准比色卡对照
(2)碱 酸 (3)洗发 护发
14、无明显变化 变红色 溶液变浑浊,颜色消失(或变浅)
三、实验探究题
15、【得出结论1】能
【质疑并求证】弱
【得出结论2】相对强弱
【拓展应用】红
柠檬酸固体不显酸性
【反思】水与二氧化碳反应生成碳酸,碳酸在水中会电离出H+ ;柠檬酸溶解于水,在水中会电离出 H+