![]()
【本讲教育信息】
一. 教学内容:
钠
二. 教学目标
1. 认识钠是一种很活泼的金属,了解钠的物理性质,掌握Na的化学性质。
2. 通过钠的性质实验及对实验现象的讨论,培养观察能力和思维能力。
三. 教学重、难点
1. 重点:
从钠的结构理解化学性质的活泼性。
2. 难点:
对钠的有关实验现象的观察和分析。
四. 知识分析
1. 钠的物理性质
首先对贮存在试剂瓶中的钠进行观察,有何发现?再将一小块钠取出,用滤纸吸干煤油,用小刀在石棉网上切下一小块,观察。
归纳为五字物理性质:软、毫、轻、低、导。
2. 钠的原子结构示意图
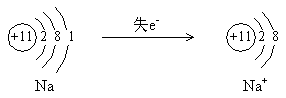
从钠的原子核外电子排布看,其最外电子层仅有1个电子,因此,极易失去,而达到稳定结构。形成阳离子(![]() )
)
由结构上的这一特点决定了![]() 的性质活泼,易失电子,具有很强的还原性。
的性质活泼,易失电子,具有很强的还原性。
3. 钠的化学性质
(1)与非金属反应
实验:![]() 在空气中燃烧
在空气中燃烧
现象:先熔成一个银色的小球,而后燃烧,发出黄色的火焰,生成淡黄色粉末状固体。
![]() (过氧化钠)
(过氧化钠)
![]()
![]()
![]()
(2)与水反应
实验:![]() 与
与![]() 的反应
的反应
现象:浮、熔、动、响、红
![]()
思考:
①
金属![]() 放入
放入![]() 溶液中发生的反应是什么?
溶液中发生的反应是什么?
②
金属![]() 放入稀盐酸中发生的反应?
放入稀盐酸中发生的反应?
③
金属![]() 在空气中就会变质,请你推测它的变化过程。
在空气中就会变质,请你推测它的变化过程。
小结:![]() 与盐溶液的反应,需先与水反应,再考虑生成的碱能否与盐反应。
与盐溶液的反应,需先与水反应,再考虑生成的碱能否与盐反应。
4. 钠的保存
常温时钠易被空气中的氧气所氧化,水及水蒸气也随之反应,所以钠应保存在煤油或封存于石蜡中。
5. 钠的存在
在自然界中只存在其化合物,主要是![]() ,还有
,还有![]() 、
、![]() 、
、![]() 等形式。自然界中无游离态
等形式。自然界中无游离态![]() 。
。
6. 钠的制取
![]() (熔融)
(熔融)![]()
7. 钠的用途
(1)制![]() (2)导热剂 (3)制稀有金属单质 (4)作电光源
(2)导热剂 (3)制稀有金属单质 (4)作电光源
【典型例题】
[例1] 将![]() 钠与
钠与![]() 硫粉迅速混合起来,并放在石棉网上加热,反应后生成的固体是( )
硫粉迅速混合起来,并放在石棉网上加热,反应后生成的固体是( )
A. 黄色固体混合物 B. 硫粉与硫化钠
C. 过氧化钠与硫化钠 D. 氧化钠与硫化钠
析:在加热反应下,![]() 既能与S化合生成
既能与S化合生成![]() ,也能与空气中的氧气反应生成
,也能与空气中的氧气反应生成![]() ,而钠是过量的,所以除生成
,而钠是过量的,所以除生成![]() 还会生成
还会生成![]() 。
。
答案:A、C
点评:本题考查![]() 的性质以及从量的角度分析可能的反应。
的性质以及从量的角度分析可能的反应。
[例2](1)用金属![]() 制取过氧化钠的化学方程式是
,现象是 。(2)用金属钠制取
制取过氧化钠的化学方程式是
,现象是 。(2)用金属钠制取![]() 通常采用下法:
通常采用下法:![]() ,不采用钠在氧气中燃烧而采用此法的原因是 ,反应中
,不采用钠在氧气中燃烧而采用此法的原因是 ,反应中![]() 作
剂,电子转移数目是 。
作
剂,电子转移数目是 。
析:第(2)问的思路是逆向思维,想一想若不用此法会产生什么样的后果,不难发现:![]() 在空气或氧气中燃烧后生成
在空气或氧气中燃烧后生成 ![]() ,而在
,而在![]() 的环境中不会被氧化为
的环境中不会被氧化为![]() 。
。
答案:(1)![]() ;黄色火焰。(2)见析;氧化;6
;黄色火焰。(2)见析;氧化;6
点评:有的问题若不能直接切入,就试着采取以退为进的方法,从条件的反面去思考,如:不这样,会怎样?
[例3] 金属钠着火时,采用的灭火物质是( )
A. 煤油 B. 砂子 C. 水 D. 泡沫灭火器
析:煤油是易燃物遇明火燃烧,水能与钠反应生成![]() ,
,![]() 也是易燃物;D喷出的物质中也有
也是易燃物;D喷出的物质中也有![]() ,这些物质不仅不能扑灭金属
,这些物质不仅不能扑灭金属![]() 的着火,而且会使火势更猛。
的着火,而且会使火势更猛。
答案:B
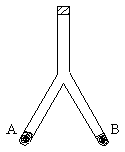
[例4] 一密闭容器,已知A端盛有![]() ,B端盛有
,B端盛有![]() ,当同时加热容器的两侧支管时,
,当同时加热容器的两侧支管时,![]() 着火燃烧,冷却后测得容器中的空气成分并未发生变化,求
着火燃烧,冷却后测得容器中的空气成分并未发生变化,求![]() 值。
值。
析:空气成分不改变说明钠燃烧消耗![]() 的量与
的量与![]() 分解放出
分解放出![]() 的量相等。
的量相等。
解:设![]() 质量为
质量为![]() ,由O原子守恒可列关系式:
,由O原子守恒可列关系式:
![]()
23 216.6
![]()
![]()
点评:当氧气充足时,应考虑![]() 燃烧生成
燃烧生成![]() ,这是开始计算的前提。
,这是开始计算的前提。
[例5](1)取一支大试管,加入![]() 的水与苯(
的水与苯(![]() ),静置。取黄豆粒大小的金属钠(
),静置。取黄豆粒大小的金属钠(![]() ),轻轻放入这支装有水和苯的试管,试推断观察到的现象是
。
),轻轻放入这支装有水和苯的试管,试推断观察到的现象是
。
(2)在实验室里,有一瓶浸在煤油里的钠块,要取用金属![]() 进行上述实验,取用的操作方法是
。
进行上述实验,取用的操作方法是
。
析:(1)钠块将落在苯和蒸馏水的界面上,有气泡产生,使钠块上浮,当附着在钠块表面的氢气逸出后,钠块又下沉到水和苯的界面上,又发生反应,重复发生上述现象直至钠反应耗尽,逐渐消失。
(2)用镊子取出钠块,用滤纸擦净表面上的煤油,在玻璃片上用小刀切去表面的氧化层,再切下一小粒备用,余下的钠全部放回试剂瓶的煤油里封存。
【模拟试题】(答题时间:30分钟)
1. 钠在自然界中存在的主要形式是( )(上海市测试题)
A. 单质 B. 氧化物 C. 氢氧化物 D. 正盐
2. 金属钠分别与下列溶液反应时,既有沉淀析出,又有气体逸出的是( )
A. ![]() 溶液 B.
溶液 B.
![]() 溶液
溶液
C. ![]() 溶液 D.
溶液 D.
![]() 溶液
溶液
3. 保存金属钠的方法是( )(成都市诊断题)
A. 放在棕色瓶中 B. 放在细沙中
C. 放在水中 D. 放在煤油中
4. 金属钠长期置于空气中,最后变为( )(北京市会考题)
A. ![]() B.
B.
![]()
C. ![]() D.
D.
![]()
5. 关于钠原子和钠离子,下列叙述错误的是( )(湖南省会考题)
A. 它们相差一个电子层
B. 它们的化学性质相似
C. 钠原子半径比钠离子大
D. 钠原子、钠离子均为同一元素
6. 钠的下列用途与钠的化学性质无关的是( )(武汉市调考题)
A. 制取过氧化钠 B. 作原子反应堆导热剂
C. 冶炼金属钛 D. 广泛应用在电光源上
7. 将一块钠投入到盛有煤油和水的试管中(煤油和水均足够多),可以观察到的现象是( )
A. 钠浮在试管中的液面上
B. 钠沉入试管中溶液的底部
C. 钠在煤油里燃烧起来
D. 钠处于水和煤油的交界处
8. 取一小块金属钠放在燃烧勺里加热,下列实验现象,描述正确的是( )
① 金属先熔化;② 在空气中燃烧,放出黄色火花;③ 燃烧后得白色固体;④ 燃烧时火焰为黄色;⑤ 燃烧后生成浅黄色固体物质。
A. ①② B. ①②③ C. ①④⑤ D. ④⑤
9. 已知钡的金属活动性处于钾和钠之间。下列反应可以实现的是( )
A. 钡可以从氯化钾溶液中置换出钾
B. 钡可以从冷水中置换出氢而得到氢气
C. 钡可以从氯化钠溶液中置换出钠
D. 在溶液中钡离子可以氧化金属锌
A. 只有![]() B.
只有
B.
只有![]()
C. ![]() 和
和![]() D.
无法确定
D.
无法确定
11. 相同质量的![]() 、
、![]() 、
、![]() 分别与足量盐酸充分反应,生成氢气的质量比为( )。(昆明市检测题)
分别与足量盐酸充分反应,生成氢气的质量比为( )。(昆明市检测题)
A. ![]() B.
B.
![]()
C. ![]() D.
D. ![]()
12. 将
A. 等于4.6% B. 等于8%
C. 小于8% D. 大于8%
13. 钠是一种硬度 ,
色的
金属(填“轻”或“重”)。在自然界中,只以
态存在,主要以 (填物质名称)的形式存在。常用作原子反应堆导热剂的是 。钠通常保存在 中,不保存在![]() 中的原因是
。(石家庄市测试题)
中的原因是
。(石家庄市测试题)
14. 新切开的金属钠,切面呈 色,在空气中很快变 ,说明钠很易 ,有关的化学方程式是 。(江苏省会考题)
15. 将小块金属钠投入盛有水的烧杯里,钠 (填“浮”、“沉”)在水面 (填“上”、“下”),有 放出。钠熔化成闪亮的小球,说明 。反应的化学方程式为 向烧杯中滴加酚酞试液,溶液呈 色,原因是 。
16. 把少量的金属钠分别放入下列溶液中,说明实验现象,并写出相应反应的离子方程式。
(1)钠放入![]() 溶液中,现象是
,离子方程式为 。
溶液中,现象是
,离子方程式为 。
(2)钠放入稀盐酸中,现象是 ,离子方程式为 。
(3)钠放入![]() 溶液中,现象是 ,离子方程式为 。
溶液中,现象是 ,离子方程式为 。
17. 将多少克钠投入

【试题答案】
1. D 2. C 3. D 4. D 5. B
6. BD 7. D 8. C 9. B 10. C
11. D 12. D
13. 很小;银白;轻;化合;氯化钠;钠和钾的合金;煤油;钠的密度比![]() 小,钠将浮在
小,钠将浮在![]() 液面上,达不到隔绝空气的作用
液面上,达不到隔绝空气的作用
14. 银白;暗;被空气里的氧气氧化生成氧化物;![]()
15. 浮;上;气体;反应放热;
![]() ;红;生成碱。
;红;生成碱。
16.
(1)钠块浮于液面,熔成小球,四处游动,![]() ,
,![]()
(2)钠块浮于液面,熔成小球,四处游动,甚至会产生黄色火球在液面上游动。
![]()
(3)钠块浮于液面,熔成小球,四处游动,产生蓝色絮状沉淀。
![]()